Scientific journal
Modern high technologies
ISSN 1812-7320
"Перечень" ВАК
ИФ РИНЦ = 1,279
APPLICATIONS OF EXTRACT OF KUKUMARIA YAPONICA FOR PROPHYLACTIC OF DISTURBANCE RELATED TO STRESS
Разработка эффективных способов повышения устойчивости к эмоциональному стрессу остается одной из актуальнейших социальных проблем современной физиологии и медицины[3,5,6,7,11,12].
В последние годы появилось много публикаций о биологической и фармакологической активности органических природных соединений морского происхождения. Из морских гидробионтов наиболее распространенным представителем в прибрежных водах Приморья является кукумария японская (Cucumaria japonica), из класса голотурий. Ткань кукумарии содержит витамины А, F, группы В, каротин, значительное количество минеральных веществ и тритерпеновые гликозиды. Тритерпеновые гликозиды, выделенные из животных, относятся к универсальным биорегуляторам, способным влиять на рост и развитие многоклеточных организмов, центральную нервную систему, кровь и кроветворение, метаболизм [2,3,8,9].
Особый интерес представляет проблема регуляции функционального состояния надпочечников, играющих ведущую роль в формировании адаптивной резистентности организма [10,12].
На базе ТИНРО - Центра г. Владивостока создана биологически активная добавка (БАД) «Тингол - 1» (гидролизат из кукумарии японской (ГКЯ), полученный ферментативным гидролизом с помощью протеолитического фермента из внутренностей краба), содержащая в своем составе тритерпеновые глигозиды (ТГ).
Цель настоящей работы. Исследование влияния гидролизата кукумарии японской на развитие реакции стресса у животных с целью выявления стресс -протективного действия.
Материалы и методы. Опыты выполнены на 50 белых беспородных крысах - самках массой 180 - 220 г, содержащихся в виварии при естественном световом режиме и свободном доступе к воде и пище. Животные были разделены на 6 групп: 1 - я - интактные; 2 - я - животные, получавшие ГКЯ (содержание ТГ 100 мкг/мл) в виде одной ежедневной добавки к основному корму в количестве 3,0 мл на 1 кг веса тела с 1,5 до 3,5 мес.; 3-я - интактные + острый стресс (контроль); 4 - я - животные, получавшие ГКЯ + острый стресс; 5 - я - интактные + стресс 12 дней (контроль); 6 - животные, получавшие ГКЯ + стресс 12 дней. Стресс моделировали опусканием животных в холодную воду при температуре 6±10С в течение часа однократно или многократно (до 12 дней по 1 разу в день) [1,5]. В настоящей работе исследовали эффект ГКЯ на стадии тревоги (однократное пребывание в воде) и стадии истощения (12 дней стресс - воздействия). После легкого эфирного наркоза крыс декапитировали. Для приготовления гистологических препаратов использовали левый надпочечник. Его извлекали тотчас после забоя, фиксировали в жидкости Карнуа. Серийные парафиновые срезы из средних слоев железы толщиной 7 мкм окрашивали гематоксилином и эозином. Учитывая, что по размерам секреторных клеток можно оценивать функциональное состояние надпочечников [11], мы измеряли площадь ядер и цитоплазмы клеток пучковой зоны коры надпочечников, а также определяли ядерно-цитоплазматические соотношения и ширину различных зон коры. Все цифровые данные обрабатывали статистически с использованием критерия Стъюдента.
Результаты исследований и их обсуждение. Микроскопическое исследование надпочечников экспериментальной группы крыс показало, что на фоне приема ГКЯ изменений надпочечников не было. В тоже время при морфометрическом анализе наблюдалось небольшое изменение соотношения различных зон коры надпочечников. Ширина пучковой зоны у экспериментальных крыс была достоверно выше, чем у интактных (таб. 1).
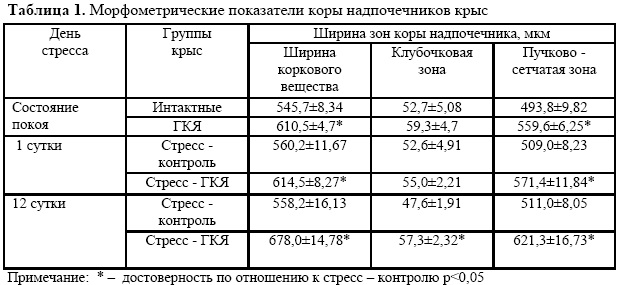
Гистологическое
изучение срезов у экспериментальных животных показало, что объемы клеток в
клубочковой и сетчатой зонах имели тенденцию к увеличению размеров. Однако в
пучковой зоне наблюдали достоверное увеличение объема цитоплазмы, так как
увеличению объема цитоплазмы сопутствовало укрупнение ядер, то ядерно -
цитоплазматические соотношения остались неизменными.
Воздействие холодом на первые сутки в стресс - контроле привело к достоверному увеличению объема ядер в пучковой зоне на 16,1%, что указывало на повышение функциональной активности надпочечников. Объем цитоплазмы достоверных изменений не имел, ядерно - цитоплазматические соотношения при этом увеличились на 12,5%. Однократное холодовое воздействие не вызывало активации клеток клубочковой и сетчатой зон и мозгового вещества. Ширина коркового вещества достоверно не изменилась (таб. 1). Относительная масса надпочечников имела тенденцию к повышению, а именно у самок с весом 149,2±1,23 г составила 15,0±0,42мг, что статистически значимо.
На фоне приема пищевых добавок с высоким содержанием тритерпеновых гликозидов мы наблюдали следующие изменения функциональной активности надпочечников.
На 1 сутки холодового воздействия у стресс-экспериментальных крыс относительная масса надпочечника у самок весом 155±3,15 г составила 16,2±0,14 мг, что достоверно выше, чем в стресс - контроле. Цитологические исследования показали, что в клубочковой и сетчатой зонах объемы ядер и цитоплазмы не изменились. Адренокортикоциты пучковой зоны не изменили своих объемов, что привело к достоверному отличию ядерно-цитоплазматических соотношений, по отношению к стресс - контрольным животным. Ширина пучково-сетчатой зоны не изменилась по отношению к стресс - контролю и была достоверно выше (таб. 1).
На 12 сутки холодового воздействия у стресс - контрольных крыс отмечали, что стрессовая гипертрофия надпочечников подвергалась редуцированию. Этот процесс характеризовался снижением объема клеток в пучковой зоне, что привело к уменьшению ширины пучково - сетчатой зоны и коркового вещества в целом (таб. 1). Эти изменения совпали со снижением относительной массы надпочечника до 15,6±0,35 мг при уменьшении массе тела до 141,8±2,56 г. Морфологическое изучение надпочечников показало, что во всех зонах коры отмечался кариопикноз и карионекроз.
Так как в результате эксперимента вес надпочечников увеличивался не постепенно, а резко, а также очень быстро наступало ослабление гипертрофии надпочечников на фоне потери веса тела и атрофии внутренних органов, то эти признаки можно оценить как начальные проявления наступающего общего истощения.
На 12 сутки холодового воздействия у экспериментальных крыс мы отметили, что сохраняется гипертрофия клеток во всех зонах коры, что привело к появлению статистически значимых отличий. Гипертрофия клеток клубочковой, пучковой и сетчатой зон достоверна по отношению к стресс - контролю, где гипертрофия клеток резко нарастала в начале эксперимента и к 12 суткам подвергалась редуцированию. Увеличение объемов клеток и высокая митотическая активность привела к умеренному расширению коркового вещества надпочечников, за счет расширения клубочковой и пучково-сетчатой зон. Прирост массы тела животных не имел тенденции к снижению на протяжении всего эксперимента. Морфологическое изучение надпочечников показало, что корковое вещество сохранило свое строение.
Таким образом, предварительный прием животными гидролизата из кукумарии японской, а также получение пищевых добавок во время стрессовой реакции увеличивает компенсаторные возможности организма. Учитывая результаты полученных исследований, можно говорить о том, что гидролизат кукумарии японской, обладая стресс-протективной активностью, способствуют формированию более выраженной стадии резистентности.
СПИСОК ЛИТЕРАТУРЫ:
1. Авакян А.Р., Лазарев А.И., Прокопенко Л.Т. // Антибиотики и химиотерапия. -2002. - Т. 47, № 2. - С. 3- 7.
2. Аминин Д.Л., Анисимов М.И. // Журн. эволюц. биохимии и физиологии. - 1990. -Т.26, №1. - С. 9-13.
3. Бодров В.А. // Психологический журнал. - 2006. - Т. 27. № 3. - С. 106 - 113.
4. Бейр Э.В., Эльбекьян К.С., Арушанян Э.Б. // Журн. высшей нервной деятельности. - 2001. - Т. 51, №5. - С. 631 - 635.
5. Гилинский М.А., Колосова Н.Г., Петракова Г.М. // Вестн. Рос. АМН. - 1998. - №10. -С.22 - 26.
6. Граевская Е.С. // Бюл. эксперим. биологии и медицины. - 2001. - Т.131, № 4. - С. 396 - 398.
7. Крылова С.Т., Коновалова О.Н., Зуева Е.П. // Эксперим. и клинич. фармакология . - 2000. - № 4. - С. 70 -74.
8. Стоник В.А. // Вестник ДВО РАН. - 1999. - №4. - С. 25-33.
9. Шарова Л.В., Седов А.М., Стоник В.А. // Фармакология и токсикология. - 1991. - Т.54, №1. - С. 60-61.
10. Gisele Cus Manfro, Carlos Alexandre Netto, Mark Pollack, Kelin Maggioni Mezzomoet al // Arq. neuron-psiquiat. - 2003. - Vol.61, №1. - P. 20 - 24.
11. Milosevic Verica, Brkic Branislava, Starcevic Vesna // Jugosloven. med. biohem. -2001. - Vol.20, №2. - P. 89 - 97.
12. Tobin, Jonn P. // Irish J. Psychol. Med. -2001. - Vol.18, №1. - P. 27 - 29.
Библиографическая ссылка
Солодкова О.А., Каредина В.С., Зенкина В.Г. ИСПОЛЬЗОВАНИЕ ГИДРОЛИЗАТА КУКУМАРИИ ЯПОНСКОЙ В ПРОФИЛАКТИКЕ НАРУШЕНИЙ, СВЯЗАННЫХ СО СТРЕССОМ // Современные наукоемкие технологии. 2009. № 9. С. 9-12;URL: https://top-technologies.ru/en/article/view?id=26535 (дата обращения: 16.05.2026).



