Введение
В последние несколько десятилетий областью интереса ученых всего мира стали нейродегенеративные заболевания (НДЗ), являющиеся ведущей причиной инвалидизации и снижения качества жизни населения. Дифференциальная диагностика нейродегенеративных нозологий представляет собой серьезную проблему в силу сходства клинической картины при разных патологических формах. Значительная вариабельность течения, даже в рамках одной нозологической формы, атипичные проявления и перекрытие симптомов также значительно осложняют диагностику нейродегенеративных заболеваний, особенно на ранних стадиях.
Нарастающее нарушение речи является типичным симптомом для нейродегенеративных заболеваний, в ряде случаев в отсутствие или при минимальной выраженности других когнитивных нарушений. В рамках диффузного поражения головного мозга речевые расстройства различной модальности (афазия, дизартрия, апраксия речи) могут встречаться в комплексе, что клинически проявляется разнообразием речевого нарушения, охватывая собой нарушения артикуляции, беглости, понимания и инициации речи, номинативные трудности, нарушения чтения и письма и другие проявления. Зачастую нарушение речи, возникающее постепенно и неуклонно прогрессирующее, выступает предиктором – первым и изолированным симптомом нейродегенеративного процесса [1]. Выявление особенностей речевого нарушения в таких случаях может сыграть большую роль для установления достоверного диагноза и выбора тактики дальнейшего лечения.
Первичная прогрессирующая афазия (ППА) – редкое заболевание, входящее в группу нейродегенеративных заболеваний и проявляющееся неуклонным прогрессированием речевых нарушений при сохранности других когнитивных функций по крайней мере в течение двух лет [2]. В дальнейшем, по мере распространения дегенеративного процесса за пределы речевых зон мозга, возможно появление специфических неврологических, когнитивных и поведенческих нарушений. За счет своего прогрессирующего, непрерывного характера ППА в итоге приводит к полному распаду речевой функции, значительному снижению социально-бытовой активности и качества жизни пациентов.
Первое клиническое описание и предложение термина «первичная прогрессирующая афазия» принадлежит американскому неврологу Марек-Марселю Месуламу. В 1982 г. он опубликовал статью «Медленно прогрессирующая афазия без генерализованной деменции» в журнале «Анналы неврологии» [3]. В ней автор описал 6 пациентов, у которых в течение 5–11 лет наблюдения преобладали речевые нарушения при отсутствии или минимальной выраженности других когнитивных нарушений.
Выделяют несколько форм ППА: логопеническую, семантическую, аграмматическую и комбинированную (смешанную). У пациентов с логопенической (англ. logopenic aphasia) формой ППА (лППА) наблюдаются трудности актуализации – подбора и называния слов и нарушение повторной речи из-за снижения объема слухоречевой памяти. При этом понимание обращенной речи, произносительная сторона и грамматическое оформление речевых высказываний у пациентов с лППА не страдают.
Семантическая (англ. fluent aphasia, semantic dementia) форма ППА (сППА) характеризуется нарушением номинативной функции речи. Пациенты затрудняются назвать предметы по показу (аномия), также нарушено понимание семантики слов. Грубо нарушается понимание и употребление более редкой, низкочастотной лексики. При этом беглость речи, повторная речь, произношение и грамматическая основа речи у таких пациентов не нарушены.
Для аграмматической (англ. non-fluent aphasia) формы ППА (аППА) характерны выраженные нарушения беглости речи, наличие аграмматизма, нарушения синтаксической стороны речи, множественные фонематические парафазии. В экспрессивной речи отмечаются запинки по типу заикания. Наблюдаются литеральные парафазии, пропуски звуков (часто флексий), звуковые искажения и персеверации. Аграмматизмы в речи проявляются в виде неправильного употребления или пропусков предлогов, местоимений, ошибок согласования, неверных окончаний, замены форм глаголов. При аППА также наблюдаются элементы импрессивного аграмматизма.
Не менее важным признаком аППА является наличие орально-артикуляционной апраксии (в неврологической практике – апраксия речи). Пациенты не могут выполнить артикуляционные движения по заданию (поцокать языком, облизать губы, вытянуть губы «трубочкой»). Параллельно страдают произношение, просодическая сторона и плавность речи. По мере прогрессирования заболевания речь пациента неуклонно ухудшается, речевая активность снижается, вплоть до полного отсутствия речи. Выделяют также комбинированную форму ППА, которая включает проявления лППА и аППА [4].
ППА диагностируется по результатам неврологического, нейропсихологического и логопедического обследования. Подтверждение клинического диагноза обеспечивается МРТ и позитронно-эмиссионной томографией в сочетании с компьютерной томографией (ПЭТ-КТ) головного мозга. Данные МРТ позволяют определить атрофические изменения в различных областях доминантного полушария. Развитие аППА связано с атрофией нижней лобной извилины (в зоне Брока) и островковой коры преимущественно левого полушария. При сППА выявляется ассиметричная атрофия в области височной доли (передних отделов). Нейровизуализационным признаком лППА являются атрофические изменения в височной и теменной долях доминантного полушария [5].
Апраксию речи, как отдельное моторное расстройство, при котором наблюдается нарушение просодической стороны речи (ритма, темпа, интонации), произносительные трудности, искажения и звуковые замены, впервые описал американский ученый Фредерик Дарли в 1967 г. [6]. Редкие случаи, при которых апраксия речи выступает ведущим и единственным симптомом нейродегенеративного процесса, выделяют в отдельный клинический синдром – первичную прогрессирующую апраксию речи (ППАР) [7]. ППАР стала рассматриваться как отдельная нозологическая форма относительно недавно. В ранних работах апраксия речи рассматривалась исключительно в рамках аППА (как один из ее клинических симптомов). Однако с накоплением научных наблюдений и исследований ППАР была выделена в отдельный синдром. Методы нейровизуализации позволяют выявить у пациентов с ППАР характерные признаки нейродегенерации в премоторных зонах лобной доли, в первую очередь в дополнительной моторной области [8].
Для ППАР характерно нарастающее нарушение моторных аспектов программирования речи, что приводит к артикуляционным и произносительным трудностям при сохранности грамматической стороны речи. По мере прогрессирования возможно присоединение афазии и дизартрии, что значительно затрудняет дифференциальную диагностику с аППА. Однако следует отметить, что при ППАР выраженность афатических нарушений не превалирует над проявлениям апраксии [9]. В клинической практике также описаны случаи прогрессирования ППАР в аППА вследствие распространения нейродегенеративного процесса из верхних премоторных областей в нижнюю лобную извилину и подкорковые структуры [10].
Выделяют три основных подтипа ППАР: фонетический (преобладают произносительные трудности), просодический (доминируют изменения просодической стороны речи – замедление темпа, увеличение пауз, нарушение интонации) и смешанный (сочетание признаков просодического и фонетического подтипов) [11]. Ключевые проявления ППАР представлены в табл. 1.
Общепринятые критерии диагностики синдрома ППАР отсутствуют, однако Х. Ботха и К. А. Йозефс предложили подтверждающие и исключающие критерии, которые приведены в табл. 2.
Согласно современным научным данным, как ППА, так и ППАР чаще всего являются клиническим предвестником развития других нейрогенедеративных заболеваний, таких как лобно-височная деменция (ЛВД), кортикобазальная дегенерация (КБД). В исследовании сотрудников ФГБНУ РЦНН представлено описание редкого клинического наблюдения пациента с первичной прогрессирующей апраксией речи с прогрессированием в кортикобазальный синдром, демонстрирующий сложности диагностики и дифференциального диагноза с близкими по патогенезу нейродегенеративными расстройствами [14]. Также описаны единичные случаи названных речевых нарушений при прогрессирующем надъядерном параличе (ПНП), а именно его речевом фенотипе (англ. progressive supranuclear palsy with predominant speech/language disorder, PSP-SL) [15].
Таблица 1
Клинические проявления ППАР
|
• Замедление общего темпа речи |
|
• Искажение и замена звуков |
|
• Усиление искажения или замены звуков при увеличении скорости произвольной речи |
|
• Слышимые или видимые артикуляционные сложности; трудности инициации речи; фальстарты |
|
• Удлинение гласных и/или согласных звуков |
|
• Повторение звуков или слогов |
|
• Сегментация слогов в словах |
|
• Увеличение продолжительности между отдельными сегментами (звуками, слогами, словами или фразами) |
|
• Распад фраз и предложений на отдельные слоги |
Примечание: составлена авторами на основе источника [12].
Таблица 2
Диагностические критерии ППАР
|
Критерии включения |
|
• Постепенное начало и прогрессирование нарушений речи |
|
• Апраксия речи является единственным или доминирующим симптомом |
|
• Дизартрия может присутствовать, однако степень ее выраженности не должна превышать выраженность апраксии |
|
• Любые симптомы афазии расценены как менее выраженные |
|
Критерии исключения |
|
• Паттерн неврологических нарушений лучше объясняется другим нейродегенеративным расстройством |
|
• Когнитивные нарушения лучше объясняются психиатрическим диагнозом |
|
• Наличие отчетливых признаков афазии, соответствующих критериям первичной прогрессирующей афазии, выявленных при детальном логопедическом/нейропсихологическом тестировании |
|
• Дизартрия превалирует над апраксией речи |
|
• Доминирующие нарушения эпизодической памяти, зрительно-пространственных функций на начальном этапе заболевания (пациент соответствует критериям типичной или атипичной болезни Альцгеймера) |
|
• Доминирующие поведенческие нарушения на начальном этапе заболевания (пациент соответствует критериям поведенческого варианта лобно-височной деменции) |
|
• Доминирующее наличие паркинсонизма, падений, глазодвигательных нарушений в начале заболевания (пациент соответствует критериям прогрессирующего надъядерного паралича) |
|
• Доминирующие идеомоторная апраксия, паркинсонизм, дистония или другие асимметричные моторные и когнитивные симптомы, включая речевые, на начальном этапе заболевания (пациент соответствует критериям кортикобазального синдрома) |
|
• Доминирующие симптомы поражения верхнего и/или нижнего мотонейрона на начальном этапе заболевания (пациент соответствует критериям болезни двигательного нейрона) |
Примечание: составлена авторами на основе источника [13].
Прогрессирующий надъядерный паралич или синдром Стила – Ричардсона – Ольшевского (ПНП) – гетерогенное заболевание, основными признаками которого являются развитие акинетико-ригидного синдрома, постуральных нарушений, псевдобульбарного синдрома (дизартрия, дисфония, дисфагия), лобного синдрома (когнитивные нарушения) и глазодвигательных нарушений (парез вертикального взора, замедление вертикальных саккад) [16]. Исследования с помощью магнитно-резонансной томографии (МРТ) пациентов с ПНП показывают атрофическое поражение в структурах ствола мозга, в частности среднего мозга, а также коры префронтальных и височных зон [17].
ПНП характеризируется прогрессирующим течением, а также полиморфностью клинических вариантов заболевания. В 2017 г. Обществом двигательных расстройств (англ. International Parkinson and Movement Disorder Society, MDS) были представлены новые диагностические критерии ПНП (MDS-PSP) и описаны различные фенотипы ПНП: фенотип Ричардсона, паркинсонический, кортикобазальный фенотип ПНП, мозжечковый, фенотип ПНП-акинезия с застываниями при ходьбе, фенотип с лобной симптоматикой и фенотип с преимущественно речевыми нарушениями [18]. Диагностика перечисленных фенотипов является сложной задачей в современной клинической практике, поскольку демонстрируются сходства с различными нейродегенеративными заболеваниями (например, с болезнью Паркинсона) или другими синдромами. Также при некоторых фенотипах на ранних стадиях развития болезни глазодвигательные и постуральные нарушения не являются преобладающими симптомами, что значительно осложняет постановку диагноза ПНП. В клинической картине речевого фенотипа на ранних этапах доминирует нарушение речи, лишь в последующем присоединяются другие симптомы ПНП [19]. Согласно клиническим критериям MDS-PSP при названном фенотипе у пациента наблюдаются речевые нарушения в виде аграмматического варианта ППА и/или апраксии речи с присоединением глазодвигательных нарушений – замедления вертикальных саккад или вертикального паралича взора. Кроме того, для ПНП характерно развитие дизартрии, которая дополнительно усугубляет состояние речи пациентов. При этом следует отметить, что диагностическая достоверность, связанная с речевым фенотипом (ППА/АР), ограничена лишь «возможным диагнозом ПНП». Однако пациенты с названным фенотипом при присоединении дополнительных клинических симптомов (постуральной неустойчивости, падений) могут соответствовать уже «вероятному» диагнозу ПНП. Таким образом, нарушение речи было признано одним из первых и ключевых клинических признаков, который может указывать на возможное развитие ПНП.
Как показывают современные исследования, более 50 % пациентов с аППА или прогрессирующей апраксией речи в последующие годы развивают другие симптомы, которые могут привести к диагнозу речевого фенотипа ПНП [20]. В 2025 г. опубликованы весьма значимые результаты исследования фенотипов, которое проводилось в период с 1998 по 2022 г. на базе Банка мозга клиники Мэйо (анг. Mayo Clinic) во Флориде (США). Исследователи провели кластерный анализ симптомов, проявляющихся у пациентов с ПНП в течение трех лет с момента начала болезни, в результате чего были выделены семь ранних подтипов заболевания, включая речевой (PSP-SL). Полученные результаты показали, что у лиц с речевым фенотипом дополнительные симптомы (паркинсонические признаки, кортикальные симптомы) развивались примерно через 4 года после начала заболевания [21].
На базе неврологического отделения второй клиники Майо в Рочестере, штат Миннесота (США), ученые описали группу из 52 пациентов с прогрессирующей апраксией речи и/или аППА, у которых на ранних стадиях заболевания практически не наблюдались симптомы, характерные для ПНП (оценивались уровень глазодвигательной функции, постуральной и общей двигательной функции). Первые признаки двигательных нарушений в виде падений, брадикинезии и глазодвигательных нарушений были отмечены только через 2 года от дебюта заболевания. По данным последующего наблюдения (через 6–6,9 лет после начала заболевания) 28 (54 %) пациентов соответствовали критериям возможного ПСП с нарушениями речи [22].
Таким образом, выявление особенностей речевых нарушений с помощью подробного логопедического обследования играет важную роль в прогнозировании возможного нозологического диагноза с целью определения прогноза заболевания и выбора терапевтической тактики. Не менее значимой является нейропсихологическая диагностика, направленная на выявление когнитивных нарушений при различных поражениях мозга, в том числе при НДЗ [23]. Условия медицинского стационара и зачастую непродолжительные сроки госпитализации обусловливают необходимость применения стандартизованных тестов и батареи (или психометрических инструментов) для диагностики. Одним из психометрических инструментов, разработанных для этих целей, является модифицированная Адденбрукская когнитивная шкала оценки когнитивных функций (Addenbrooke’s Cognitive Examination – Revised, ACE-R). Данная шкала валидизирована [24], обладает высокой чувствительностью и специфичностью в отношении когнитивных нарушений, независимо от их нозологической природы. Итоговая максимальная оценка по шкале – 100 баллов. Результат 88 и выше считается нормой (или говорит о возможном наличии недементных когнитивных расстройств), ниже 88 – подозрение на когнитивные нарушения (чувствительность 94 %, специфичность 89 %), результат ниже 82 указывает на высокую вероятность деменции (чувствительность 84 %, специфичность 100 %).
В качестве иллюстрации приводим собственное клиническое наблюдение пациентки, у которой в течение нескольких лет дебютирующим и единственным симптомом являлось нарастающее нарушение речи, в отсутствие других двигательных и когнитивных нарушений.
Цель исследования – описание редкого клинического случая пациентки с прогрессирующими изолированными речевыми нарушениями, проявляющимися в виде доминирующей апраксии речи и менее выраженными признаками аграмматического варианта первичной прогрессирующей афазии в дебюте заболевания, и обсуждение сложностей дифференциальной диагностики при выявлении нейродегенеративных причин данного расстройства.
Клиническое наблюдение
Пациентка Ч., 66 лет, женщина, правша. Образование высшее, в настоящее время на пенсии. Сбор анамнеза затруднен ввиду выраженных речевых нарушений, частично собран со слов пациентки и данных предоставленной медицинской документации. Впервые нарушения речи появились в начале 2018 г., в возрасте 59 лет. Пациентка заметила, что в длинных словах стала переставлять слоги, путать окончания, речь стала замедленной. Нарушение речи пациентка связывала с перенесенным стрессом. Спустя несколько месяцев нарушения усилились и с тех пор продолжают медленно и неуклонно прогрессировать. Назначалась нейрометаболическая терапия – без эффекта. В связи с речевыми нарушениями в 2020 г. пациентка вышла на пенсию. В октябре 2021 г. заподозрен синдром первичной прогрессирующей афазии, назначался мемантин с кратковременной положительной динамикой, после чего отмечалось ухудшение самочувствия, в связи с чем препарат был отменен. Проводился дифференциальный диагноз с функциональным речевым расстройством, консультирована психиатром, данных за функциональную природу расстройства не выявлено. Выраженность речевых нарушений нарастала, с 2023 г. заметно нарушилась коммуникативная функция речи, речь пациентки перестали понимать окружающие. С начала 2024 г. наблюдается в ФГБНУ РЦНН с диагнозом «Нейродегенеративное заболевание: первичная прогрессирующая афазия, аграмматический вариант, код по МКБ: G31.9», проходит регулярные курсы нейрометаболической терапии и занятий с логопедом. Люмбальная пункция для исследования ликворных биомаркеров болезни Альцгеймера не проводилась. В 2024–2025 гг. речевая функция продолжила постепенно ухудшаться. В 2025 г. отмечалось три последовательных эпизода выраженного головокружения (по типу системного), с ощущением «дискомфортной, шальной» головы, появилась неустойчивость при ходьбе с ощущением тенденции к падениям, непостоянное двоение в глазах. Выраженность данных симптомов постепенно нарастает. В настоящее время пациентка в самообслуживании не ограничена, самостоятельно справляется с бытовыми обязанностями, хорошо ориентируется на местности, регулярно посещает логопедические занятия (1 раз в неделю). Нарушений памяти, трудностей при ориентировке, изменения поведения за все время течения заболевания не отмечалось.
По данным обследования: молекулярно-генетическое исследование экспансии в гене C9orf72: число тандемных гексануклеотидных G4C2-повторов в обоих аллелях гена соответствует норме. Генотипирование гена AРОE (29.03.2024): генотип E3/E3.
МРТ головного мозга (2025 г.): определяется некоторое неравномерное (слева более выраженное) уменьшение объема извилин лобных долей обоих полушарий большого мозга, асимметрия гиппокампов (левый гиппокамп короче и более круглой формы), а также хориоидальных щелей (R>L); боковые желудочки слабо асимметричны (левый шире правого), неравномерно умеренно расширено субарахноидальное пространство лобных долей полушарий большого мозга и сильвиевые щели (более выраженно слева), слабо расширено – височных долей (по шкале МТА 1-2). Заключение – МРТ-данные соответствуют очаговым изменениям в обоих полушариях большого мозга, вероятнее всего сосудистого генеза. МРТ-картина неравномерного расширения ликворных пространств и неравномерного уменьшения объема извилин, при наличии соответствующих клинических данных может соответствовать нейродегенеративному процессу с преимущественным поражением лобных долей.
Томограмма, указывающая на ассиметричную атрофию левой лобной и верхних отделов височной доли (указано стрелками), представлена на рисунке.
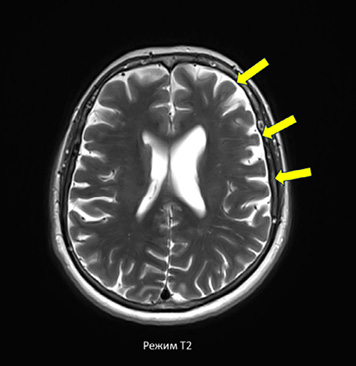
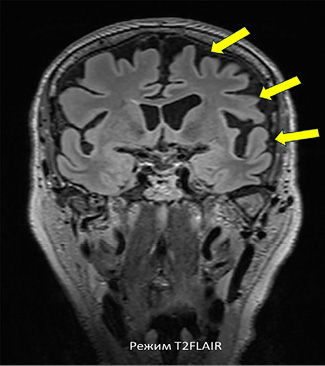
МР-томограмма головного мозга (в режимах T2 и Т2 FLAIR) больной Ч., 67 лет, с аППА Примечание: составлен авторами по результатам данного исследования
Неврологический статус на момент поступления (2026 г.): В сознании, ориентирована правильно. Контакт значительно затруднен ввиду речевых нарушений, общение в основном посредством письма (письменная речь с единичными аграмматизмами, в преобладающем большинстве – грамматически правильная). Экспрессивная речь представлена отдельными словами, присутствуют признаки апраксии речи. Четких нарушений понимания обращенной речи нет. Хватательный рефлекс с двух сторон. Элементы конечностно-кинетической апраксии в руках, идеомоторная апраксия в обеих руках. Оценка когнитивных функций по АСЕ-III: 84/100 баллов (внимание и ориентация 18/18, память 25/26, речевая активность 3/14, речь 22/26, зрительно-пространственные функции 16/16). Оценка по FAB (батарея лобной дисфункции): 17/18 баллов. Оценка по ГШТД: уровень тревоги – 2 балла (норма), уровень депрессии – 0 баллов (норма). Нейропсихиатрический опросник (NPI-Q) 0/144 баллов. Обоняние субъективно сохранно. Ориентировочно поля зрения не изменены. Глазные щели, зрачки равные. Ограничение вертикального взора, взор в крайних отведениях по горизонтали не удерживает. Лицо симметрично, апраксия верхней порции мимической мускулатуры (не нахмуривает, не поднимает брови ни по команде, ни по подобию). Грубая дизартрия, дисфония, элементы дисфагии. Рефлекс Маринеску – Радовичи с двух сторон S > D. Язык по средней линии. Четких парезов нет. Достоверная оценка мышечного тонуса затруднена ввиду паратоний, складывается впечатление о наличии легкого пластического тонуса в обеих ногах. Сухожильные рефлексы живые, равные. Кистевой аналог рефлекса Россолимо слева. Легкая двусторонняя брадикинезия без четкой разницы сторон. Гиперкинезов на момент осмотра нет. Четких расстройств поверхностной и глубокой чувствительности не выявлено. Координаторные пробы выполняет удовлетворительно. В пробе Ромберга устойчива. В пробе Тевенара ретропульсии. Походка несколько неустойчивая, передвигается без дополнительной опоры. Функции тазовых органов контролирует.
Консультация логопеда: На момент обследования больная (правша, пенсионер, до выхода на пенсию работала учителем начальных классов, не работает, инвалидности нет) ориентирована в месте, времени и собственной личности, вербальный контакт затруднен по причине выраженных речевых нарушений. Предъявляет жалобы на замедленность речи и движений, дрожание левой щеки, нарушение речи и изменение голоса, неустойчивость при ходьбе, приступы головокружений, снижение слуха, эмоциональную лабильность, сухость во рту. Со слов больной, люди стали ей говорить, что у нее «стеклянные глаза» и она «сумасшедшая» из-за речевых проблем. У больной отмечается достаточная критика к своему состоянию. В процессе обследования мотивирована, эмоционально лабильна, отмечаются эпизоды насильственного смеха. Темп выполнения заданий замедленный.
Слух объективно нарушен, нейросенсорная тугоухость 2-й степени, обоняние ориентировочно не нарушено. Лицо симметрично в покое и при выполнении мимических проб, отмечается наличие хоботкового рефлекса при введении в полость рта ложки, логопедического зонда, шпателя; гипомимия. Отмечается выраженная орально-артикуляционная апраксия. Затруднено выполнение проб на поднимание бровей, нахмуривание; пробы на надувание и втягивание щек, оскаливание зубов доступны с персеверациями. Сила жевательной мускулатуры сохранна, круговая мышца губ ослаблена. Язык – по средней линии, без налета, корень языка не тоничен. Амплитуда движений языка снижена, язык беспокойный в полости рта и при выведении. Мягкое небо при фонации и на «твердой атаке» сокращается недостаточно.
Понимание ситуативной, диалогической и некоторых форм внеситуативной речи не страдает, при общении смотрит на артикуляцию собеседника. Вербальное общение крайне затруднено, за исключением простых по слоговой структуре слов, наиболее доступен диалог. Общается преимущественно посредством письма (с единичными аграмматизмами, на письме речь грамматически правильная). Экспрессивная речь представлена отдельными словами, единичные аграмматизмы и вербальные парафазии. Отмечаются эхолалии, замены звуков по акустическому признаку, оглушение звонких согласных, редукция звуков и окончаний слов. Больная практически не применяет в речи предлоги, отмечается «телеграфный» стиль общения.
В процессе фонации речевой выдох укорочен, темпо-ритмическая организация речи нарушена, отмечается отсутствие ударений, монотония, наличие длительных пауз перед любым ответом. Голос слабомодулированный, дрожащий, прерывающийся. Пиковое время максимальной фонации снижено. Разборчивость речи и речевая активность резко снижены. Память не снижена, инструкции на выполнение нейропсихологических проб выполняет верно. Письменная речь значительно опережает устную.
Таблица 3
Результаты скринингового тестирования пациентки по шкалам за 2025–2026 гг.
|
Скрининговая шкала |
Дата проведения обследования |
|
|
14.01.2025 |
12.02.2026 |
|
|
АCE-R (общий балл) |
92/100 |
84/100 |
|
АCE-R (Внимание и ориентация) |
18/18 |
18/18 |
|
АCE-R (Память) |
25/26 |
25/26 |
|
АCE-R (Зрительно-пространственные функции) |
16/16 |
16/16 |
|
АCE-R (Речевая активность) |
10/14 |
3/14 |
|
АCE-R (Речь) |
23/26 |
22/26 |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
Заключение: аграмматический вариант первичной прогрессирующей афазии в сочетании с дизартрией грубой степени выраженности, дисфонией и дисфагией легкой степени на фоне прогрессирующей орально-артикуляционной апраксии. Рекомендовано проведение логопедических занятий.
Консультация психиатра: Органическое расстройство личности на фоне основного заболевания. В настоящее время в назначении психотропной терапии не нуждается.
В настоящее время в клинической картине пациентки доминируют выраженные речевые нарушения. При этом нарушения речи были единственными с момента дебюта заболевания (2018 г.) и в течение последующих шести лет, при отсутствии каких-либо двигательных и поведенческих нарушений, а также нарушений эпизодической памяти. При оценке паттерна речевых нарушений у пациентки наблюдается отчетливое доминирование апраксии речи с выраженными в значительно меньшей степени элементами моторной афазии, что не соответствует аППА, при которой выраженные аграмматизмы являются обязательным критерием диагностики (по М. Л. Джорно-Темпини) и позволяет предположить синдром ППАР (смешанный тип) в первые годы течения заболевания. Имеющиеся у пациентки звуковые искажения, замены, персеверации, нарушение плавности речи в виде сегментации звуков и слогов в словах, а также замедление темпа речи соответствуют проявлениям ППАР (по Х. Ботха и К.А. Йозефс).
С целью углубленного исследования речевого дефицита, помимо комплексного психолого-логопедического обследования, применялись следующие диагностические методы:
1) критерии Международной статистической классификации болезней и проблем, связанных со здоровьем, 10-го пересмотра (МКБ-10) [25];
2) Адденбрукская когнитивная шкала, ACE-R;
3) магнитно-резонансная томография (МРТ) головного мозга.
При скрининговом тестировании (в динамике за 2025–2026 гг.) по Адденбрукской когнитивной шкале (ACE-R) получены следующие баллы, представленные в табл. 3.
Как видно из табл. 3, в течение последнего года наблюдается изолированное снижение показателей речевой активности (по шкале ACE-R), при сохранности других компонентов психической деятельности. Кроме того, спустя 6 лет от начала заболевания (в 2025 г.) у пациентки отмечается присоединение экстрапирамидного синдрома с постуральными и глазодвигательными нарушениями, дизартрией, дисфонией и дисфагией. Примечательно, что с пациенткой на протяжении четырех лет проводились систематические логопедические занятия (1 раз в неделю), тогда как медикаментозная терапия (в отношении стимуляции головного мозга) была отменена из-за индивидуальной непереносимости препаратов. Таким образом, можно сделать вывод о высокой мотивации, нейропластичности и реабилитационном потенциале пациентки Ч.
Заключение
Представленное клиническое наблюдение демонстрирует редкий случай первичной прогрессирующей апраксии речи и возможную эволюцию клинической картины при длительном течении заболевания. В данном случае представлен пример прогрессирования ППАР в формирующийся фенотип прогрессирующего надъядерного паралича с преимущественно речевыми нарушениями. Таким образом, выявление особенностей речевых нарушений на ранних стадиях болезни имеет важное значение для установления клинического диагноза, определения прогноза и выбора тактики речевой реабилитации при нейродегенеративных заболеваниях.
Конфликт интересов
Финансирование
Библиографическая ссылка
Бердникович Е. С., Малич Т. ПЕРВИЧНАЯ ПРОГРЕССИРУЮЩАЯ АПРАКСИЯ РЕЧИ В ДЕБЮТЕ ФОРМИРУЮЩЕГОСЯ РЕЧЕВОГО ФЕНОТИПА НАДЪЯДЕРНОГО ПАРАЛИЧА: КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ // Современные наукоемкие технологии. 2026. № 4. С. 173-182;URL: https://top-technologies.ru/ru/article/view?id=40745 (дата обращения: 10.05.2026).
DOI: https://doi.org/10.17513/snt.40745



