Триазавирин – оригинальное отечественное лекарственное вещество противовирусного действия. Ведется разработка твердых лекарственных форм препарата. На сегодняшний момент зарегистрирована капсулированная форма триазавирина. Одним из этапов создания лекарственных препаратов является разработка методов его качественного и количественного анализа. Высокоэффективная жидкостная хроматография (ВЭЖХ) широко применяется в фармацевтическом анализе благодаря своей высокой чувствительности и эффективности разделения, мягким условиям анализа, автоматизации проведения испытаний [2, 4]. Цель исследования – подтвердить возможность использования обращено-фазовой жидкостной хроматографии для определения триазавирина в капсулированной лекарственной форме.
Хроматографический эксперимент проводился на хроматографе «Agilent 1200», снабженном спектрофотометрическим детектором на диодной матрице.
Условия хроматографирования триазавирина:
1) хроматографические колонки Zorbax eclipse XDB C18 5 мкм 4.6·150 мм и Separon SGX NH2 7мкм 4,6·250;
2) элюент «ацетонитрил-0,025М водный раствор ацетата натрия» в соотношении 10:90 по объему при использовании обеих колонок;
3) расход элюента 850 мкл/мин;
4) длина волны детектирования 215 нм;
5) объем пробы 5 мкл;
6) проба: 0,025 г (точная навеска) модельной смеси, растворенной в 25 мл элюента;
7) температура окружающей среды 22 ±2 °С.
Обсуждение результатов. Пригодность хроматографических колонок для количественного определения триазавирина.
Первоначально проводился выбор хроматографической колонки по разделяющей эффективности. Для каждой из них рассчитывалось число теоретических тарелок (ЧТТ) как функция времени удерживания и ширины пика основного компонента (табл. 1) [4].
Таблица 1
Эффективность хроматографических колонок
|
Хроматографическая колонка |
Zorbax eclipse XDB C18 5 мкм 4.6*150 мм |
Separon SGX NH2 7мкм 4,6*250 |
|
Эффективность,N |
34438 |
19600 |
|
Разрешение,R |
38,22 |
16,52 |
Эффективность хроматографической колонки N, рассчитанная по пику основного компонента (триазавирин), должна быть не менее 3500 теоретических тарелок, разрешение R между пиком 3-метилтио-5-амино-1,2,4-триазола (основная примесь) и пиком триазавирина должно составлять не менее 5,0 мин. [3].
Дальнейшая апробация методики количественного определения триазавирина в капсулированной форме проводилась на хроматографической колонке Zorbax eclipse XDB C18, как наиболее эффективной. Колонка Separon SGX NH2 оказалась непригодна для анализа триазавирина из-за нестабильности, в сторону уменьшения времен удерживания.
Определение метрологических характеристик методики количественного определения триазавирина. Точность аналитической методики (precision) оценивалась по сходимости результатов (precision) определения триазавирина в модельных смесях в концентрации, близкой к номинальной (0,25 г). Исследовалось 5 растворов триазавирина, приготовленных независимо друг от друга в соответствии с тестируемой методикой. Каждый раствор хроматографировали 3 раза. По результатам эксперимента определялись следующие метрологические характеристики сходимости методики: средний результат (xср), относительное стандартное отклонение (srср), относительный доверительный интервал среднего результата (εср), средняя относительная погрешность определения (erср). Расчетное значение t-критерия Стьюдента должно быть меньше табличного или srср ≤2,0 % (табл. 2) [1, 5].
Таблица 2
Определение точности методики количественного определения триазавирина
|
№ р-ра |
Площадь пика, S |
Xiср,г |
Хср,г |
srср, % |
εср |
erср, % |
|
1 |
2 |
3 |
4 |
5 |
6 |
7 |
|
1 |
1238,097 1231,887 1243,201 |
0,2627 |
0,2566 |
1,59 |
0,009 |
3,5 |
|
2 |
1186,699 1193,708 1198,989 |
0,2584 |
||||
|
3 |
1198,971 1204,093 1203,003 |
0,2527 |
||||
|
4 |
1214,503 1202,053 1209,061 |
0,2557 |
||||
|
5 |
1168,424 1169,408 1160,365 |
0,2534 |
Аналитическая методика определения триазавирина признана точной по критерию сходимости результатов.
Особое внимание уделялось определению линейности методики (linearity)– способности методики в диапазоне применения давать величины сигнала Yi (площадь пика) прямо пропорциональные концентрации Сi определяемого вещества. Для оценки линейности готовилось 7 растворов с концентрациями триазавирина, охватывающими всю область действия методики (60-135 %)[5]. Данные позволяют судить о стойкой линейной зависимости между показателями концентраций триазавирина и площадями пиков (рисунок).
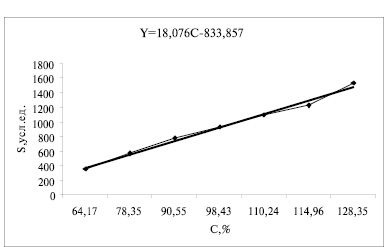
Корреляция концентраций триазавирина и площади пиков. R=0,99553
Вывод
Подтверждена возможность количественного определения триазавирина по выбранной аналитической методике на жидкостном хроматографе серии «Agilent 1200».
Библиографическая ссылка
Шаблакова А.С., Ковалев И.С., Русинов В.Л., Уломский Е.Н., Петров А.Ю. МЕТОДИКА АНАЛИЗА КАПСУЛИРОВАННОЙ ФОРМЫ ПРОТИВОВИРУСНОГО СРЕДСТВА ТРИАЗАВИРИН // Современные наукоемкие технологии. 2014. № 2. С. 93-95;URL: https://top-technologies.ru/ru/article/view?id=33659 (дата обращения: 27.03.2026).



