В новых условиях глобализации мировой экономики, вопросы охраны окружающей среды и экологической безопасности стали весьма актуальными и требующими пристального внимания всего мирового сообщества. Стало очевидным, что деятельность и дальнейшее развитие любой крупной отрасли, независимо от их принадлежности (частная или государственная), тесно взаимосвязаны с таким приоритетным направлением, как обеспечение экологической безопасности.
За годы независимости в Казахстане создана и действует совершенно новая государственная система обеспечения экологической безопасности, управления охраны окружающей среды и природопользования с хорошо организованной и территориально разветвленной системой исполнительных органов, призванных обеспечить охрану окружающей среды. Однако с учетом того, что на протяжении многих десятилетий в Казахстане складывалась преимущественно сырьевая система природопользования с экстремально высокими техногенными нагрузками на окружающую среду, кардинального улучшения экологической ситуации пока не произошло. Она по-прежнему характеризуется дестабилизацией природной системы, ведущей биосферу к утрате ее способности поддерживать качество окружающей среды, необходимое для жизнедеятельности общества.
Именно поэтому экологическая безопасность, как одна из основных стратегических компонентов обеспечения национальной безопасности Республики Казахстан, стала одной из ключевых задач, требующих безотлагательного решения.
Реформирование всех отраслей национальной экономики стало основой изменения отношения к использованию природных ресурсов для осуществления социально-экономического устойчивого развития общества с учетом сохранения положительного импакт-фактора окружающей среды. При этом, в Казахстане в качестве первого стратегического направления по переходу страны к «зеленой экономике» выделена стабилизация и улучшение качества окружающей среды, обеспечение экологической безопасности населения от деятельности металлургических предприятий и угольных тепловых электростанций.
Глубокий анализ современного состояния этих ключевых отраслей экономики Казахстана показывает, что в результате деятельности данного сектора экономики с каждым годом усиливается тенденция истощения запасов первичного сырья при невозобновляемости рудного сырья, необходимости энерго-, ресурсосбережения, нарастания экологических проблем и самое главное – дефицита земли, требуемой для захоронения новых образующихся промышленных отходов.
Состояние и актуальные вопросы энергетики
Сегодня энергетический комплекс Республики Казахстан, являясь, по существу, локомотивом отечественной экономики, выступает одним из законодателей в проведении инновационной и внешнеэкономической политики страны. Поэтому понимание перспективы развития и дальнейшего совершенствования энергетической отрасли не вызывает сомнений и требует пристального внимания к нему.
Разделяя общий тренд суждений известных ученых о перспективности развития энергетической отрасли, в данной статье высказывается мнение, которое могло бы стать, на наш взгляд, принципиальным толчком в решении основного концептуального вопроса для отрасли – глубокой очистки отходящих газов от сернистого ангидрида и других вредных выбросов. Без решения данного вопроса в новых условиях уже не должно быть и речи о возможности развития производственной деятельности ни одного промышленного предприятия… Причем, одной из наиболее серьезных проблем, возникающей при сжигании угля на предприятиях энергетической отрасли, является загрязнение воздуха диоксидом серы. Сернистый ангидрид оказывает существенное негативное влияние на флору [2]. Наиболее чувствительны к нему хвойные и лиственные леса. Так, воздействие даже незначительных концентраций (0,23–0,32 мг/м3) диоксида серы на хвойные массивы приводит к их усыханию в течение 2–3 лет. Заметные изменения лиственных пород наступают при концентрации сернистого ангидрида 0,5–1,0 мг/м3. Хроническое воздействие сернистого ангидрида на органы дыхания способствует возникновению бронхитов, в ряде случаев с астматическими явлениями за счет спазмы, а также других респираторных заболеваний.
По данным статистического анализа ряда промышленных стран [1], ежегодный выброс сернистого ангидрида от сжигания каменного угля, содержащего в среднем 0,7–1,5 % серы, составляет около 45–54 млн т.
В Италии сернистого ангидрида выбрасывается около 3 млн т, в том числе от сжигания топлива – 89 %. В Великобритании выбросы сернистого ангидрида составляют 5–6 млн т (в основном от сжигания топлива). Основным источником выбросов сернистого ангидрида в США являются электростанции, использующие уголь, на долю которых приходится 45 % суммарной величины выброса по стране.
По мнению европейских экспертов, мировой рынок электроэнергетики находится на пороге перехода с газа на уголь, как наиболее предпочтительный вид топлива для тепловых электростанций [8]. Именно поэтому уже сегодня во всем мире идет активный поиск технологий и оборудования для утилизации отходящих газов при соблюдении современных требований экологии.
Относительно энергетической отрасли Казахстана, промышленные выбросы предприятий в атмосферу составляют порядка трех миллионов тонн в год, из которых 85 % приходится на 43 крупные тепловые угольные электростанции и металлургические производства. При этом выбросы тепловых электростанций составляют до 70 % от общего объема эмиссий энергетического комплекса и 43,7 % – от эмиссии загрязняющих веществ в атмосферу [3]. В выбросах различных источников Единой энергетической системы доминируют твердые частицы – 35 %, диоксид серы – 31 %, оксиды углерода и азота – 19 % и 14 % соответственно [4]. По имеющимся данным, предприятия ТЭЦ Казахстана, работающие преимущественно на углях с высоким содержанием серы (до 0,7 %) и золы (до 50 %), имеют КПД на уровне 33–35 %. Объекты электроэнергетики, построенные в 50-е и 70-е годы прошлого столетия, практически выработали производственный ресурс. Коэффициент износа основного электрооборудования, по предварительным расчетам на 2010 г., составляет 82 % [5].
В настоящее время на большинстве предприятий энергетической отрасли очистка отходящих газов угольных электростанций от газообразного SO2 выполняется старыми способами, основанными на взаимодействии потока отходящего газа с известняком – CaCO3 или гашеной известью – Са(ОН)2, которые могут быть в твердом виде или в виде водной суспензии. Эти методы недостаточно эффективны и обладают рядом недостатков: высокое остаточное содержание серы в газах (в лучшем случае 90 % SO2 удаляется из отходящих газов при его исходном содержании около 2 %); процессы довольно дорогие (при их применении стоимость электричества может увеличиться на несколько десятков процентов); большой выход неиспользуемых твердых отходов (в основном загрязненного примесями от сгорания угля, гипса – CaSO4), количество которых составляет несколько процентов от веса сжигаемого угля [1, 6, 7].
Отсутствие надежной системы очистки дымовых газов и использование старых методов улавливания SO2 и других вредных загрязнителей атмосферы привели к возрастанию их концентраций в выбросах выше предельно допустимых норм. По данным статистики, из всего количества источников выбросов загрязняющих веществ, имеющихся в республике, очистными сооружениями оборудовано всего лишь около 10 % источников.
Ныне уровень среднегодовой концентрации сернистого ангидрида в воздухе крупных городов Казахстана от сжигания топлива в промышленных и бытовых установках уже достигает ~ 1,0 мг/м3 [5]. Отсюда следует вывод о том, что основная причина отрицательного воздействия на окружающую среду и жизнедеятельность человека состоит не столько в росте производства, сколько в отсутствии комплексной переработки полезных ископаемых и больших объемов отходящих газов, содержащих вредные компоненты.
Проведенный анализ позволяет сформулировать основные требования, предъявляемые при разработке новых технологий по очистке отходящих газов ТЭЦ и металлургических предприятий. В условиях наблюдаемого роста концентраций SO2 и других вредных выбросов в отходящих газах ТЭЦ и металлургических предприятий Казахстана и отсутствия надежной технологии очистки отходящих газов, требуется создание новых современных технологий глубокой очистки отходящих газов, которые могли бы обеспечить:
? низкое остаточное содержание серы в отходящих газах после очистки (до остаточного содержания серы 0,001 %);
? получение серы в форме, позволяющей ее дальнейшее использование для получения товарной продукции – серной кислоты или элементарной серы;
? безотходность технологии.
С учетом этих реалий вполне очевидно, что разработка технологии, адаптированной к условиям производства действующих тепловых электростанций, направленной на снижение эмиссий вредных веществ в окружающую среду является актуальной задачей и полностью отвечает приоритетным направлениям научного, научно-технического и социально-экономического устойчивого развития Республики Казахстан.
В настоящей работе приводятся теоретические и практические основы новой альтернативной технологии очистки отходящих газов ТЭЦ от сернистого ангидрида, а также выборочные результаты комплексных исследований, проводимых учеными КазНИТУ имени К.И. Сатпаева и Научного института имени Вейцмана (Израиль) в тесной кооперации с инженерно-техническими работниками АО «Энергоорталык-3».
Физико-химические основы технологии
Суть выбранной к разработке технологии заключается в том, что поглощение SO2 отходящих газов осуществляется расплавленной эвтектической смесью карбонатов щелочных металлов (лития, натрия и калия) при низких температурах (450–650 °С) по реакции
Me2CO3 + SO2 = Me2SO3 + CO2. (1)
Полученный сульфит в результате окисления кислородом переходит в сульфат (Me2SO4):
Me2SO3 + 0,5O2 = Me2SO4,
где
Me = Li, Na, K. (2)
Используемая в процессе исходная эвтектическая карбонатная смесь содержит, %: Li2CO3 – 43,5, Na2CO3 – 31,5, K2CO3 – 25,0. Температура плавления эвтектической смеси 395 °C. При температуре ведения процесса (выше 450 °C) смесь имеет низкую вязкость.
В условиях ведения процесса (при температуре выше 450 °С) протекание реакции (2) проходит на границе капель карбонатного расплава и потока газа, подаваемого снизу. При резком росте столкновений молекул SO2 c поверхностью карбонатного расплава следует ожидать достаточно высокой скорости протекания реакции (2) – поглощения серы карбонатным расплавом с образованием сульфатов щелочных металлов. Данным явлением объясняется и относительно малое количество карбонатного расплава, необходимое для удаления SO2 из газов. Как показали результаты предварительных расчетов, при работе тепловых станций мощностью 335 МВт для удаления SO2 из отходящих газов необходимо относительно небольшое количество расплава ~ 10 м3. При этом остаточное содержание SO2 в газах после очистки будет составлять ~ 0,003 %. Это в 15 раз ниже, чем при использовании наиболее эффективных процессов на основе известняка.
После поглощения газов SO2 расплав содержит в основном сульфаты щелочных металлов, растворенные в эвтектической смеси карбонатов. Расплав карбонатов, содержащий сульфаты и небольшое количество сульфитов, регенерируется с получением товарных продуктов – серы или серной кислоты.
Таким образом, в работе предлагается новое решение удаления серы из карбонатно-сульфатного расплава – путем восстановления его угарным газом – СО. Химический процесс регенерации основан на извлечении серы из расплава в наиболее удобной ее форме – в виде карбонилсульфида (COS), пригодной для получения серной кислоты или элементарной серы.
Предлагаемая технология обеспечивает решение двух очень важных вопросов для практики: (а) повышение срока эксплуатации оборудования (при 550 °C воздействие сульфатно-карбонатного расплава на оборудование минимально); (б) обеспечение возможности удаления серы в наиболее удобной форме COS, пригодной для выбора и получения конечного продукта – серной кислоты или элементарной серы.
Отличительной особенностью новой технологии является возможность ведения процесса химической абсорбции сернистого ангидрида и регенерации карбонатно-сульфатного расплава при одинаковых температурных режимах – 450–600 °C. Незначительный перепад рабочих температур позволяет проводить процессы абсорбции газов карбонатными расплавами щелочных металлов и дальнейшей регенерации полученных сульфатно-карбонатных расплавов в одном аппарате.
Описанные выше механизмы процесса абсорбции SO2 карбонатным расплавом и дальнейшей регенерации сульфатно-карбонатного расплава монооксидом углерода основаны на результатах термодинамических расчетов.
Термодинамические расчеты сводились к определению изобарно-изотермических потенциалов (свободная энергия Гиббса, ?GT) возможных реакций взаимодействия компонентов карбонатного расплава щелочных металлов с отходящими газами от температуры. В основу расчетов положен метод минимизации полного потенциала энергии Гиббса.
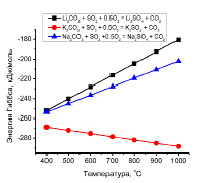
Рис. 1. Изменение свободной энергии Гиббса (?GТ) реакций взаимодействия карбонатов щелочных металлов со смесью SO2 и O2 от температуры
Расчеты энергии Гиббса (?GТ) принятых к термодинамическому анализу реакций проводили при стандартном состоянии чистый переохлажденный жидкий карбонат (Me2CO3 liquid) и сульфат (Me2SO4 liquid) щелочного металла. Исходные данные для расчетов получены из работы [9] и веб-сайта NIST-JANAF Thermo chemical Tables.
Результаты термодинамических расчетов значений свободной энергии Гиббса (?GТ) реакций взаимодействия компонентов расплавленных карбонатов щелочных металлов со смесью SO2 и O2 в температурном интервале 400…1000 °C показали высокую термодинамическую вероятность (рис. 1).
На рис. 1 видно, что для реакций взаимодействия карбоната лития и натрия со смесью сернистого газа и кислорода значения энергии Гиббса с увеличением температуры снижаются и имеют идентичный характер. Это свидетельствует о том, что при взаимодействии отходящих газов со смесью карбонатного расплава возможность образования сульфата лития и сульфата натрия равнозначны. Нетрудно видеть, что с увеличением температуры направление и скорость реакции взаимодействия карбоната калия с SO2 сильно сдвигается в сторону образования сульфата калия (рис. 1). Более высокое значение энергии Гиббса ?G = – 270 кДж/моль данной реакции при температуре 500 °C, чем значения ?G500 °C для реакций образования сульфатов натрия и лития, свидетельствует о предпочтительности протекания реакции с образованием сульфата калия.
В целом, полученные данные позволяют сделать вывод о том, что в условиях ведения процесса химической абсорбции взаимодействие серосодержащих отходящих газов с карбонатным расплавом щелочных металлов сопровождается образованием сульфатно-карбонатного расплава, в котором содержание сульфата калия является доминирующим.
Химизм процесса регенерации – взаимодействия сульфатов щелочных металлов с монооксидом углерода (СО) – можно описать протеканием следующих реакций:
Me2SO 4 liquid + 4COgas → Me2CO3 liquid + COSgas + 2CO2gas, (3)
Me2SO 4 liquid + 4COgas→ Me2S liquid + 4CO2gas. (4)
Результаты термодинамических расчетов свободной энергии Гиббса реакций (3), (4) в температурном интервале 400…1000 °C, выполненные при стандартных состояниях: чистый переохлажденный жидкий сульфат, сульфид и карбонат щелочного металла, – показали принципиальную термодинамическую возможность восстановления чистых жидких сульфатов щелочных металлов до своих карбонатов и сульфидов с образованием в газовой фазе карбонилсульфида (COS) и диоксида углерода (СО2) (рис. 2–4).
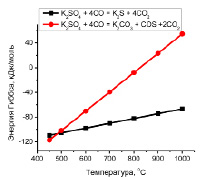
Рис. 2. Зависимость величины свободной энергии Гиббса от температуры для реакций восстановления сульфата калия монооксидом углерода
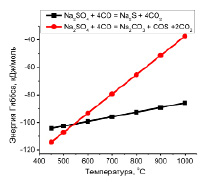
Рис. 3. Зависимость величины свободной энергии Гиббса от температуры для реакций восстановления сульфата натрия монооксидом углерода
Сравнительный же анализ расчетных значений свободной энергии Гиббса для реакций восстановления чистых жидких сульфатов калия, натрия и лития монооксидом углерода, полученных при низких температурных интервалах 400–650 °C, показывает, что:
– при температурах ниже 450 °C термодинамическая вероятность восстановления сульфата калия по реакции (3) выше, чем по реакции (4);
– для сульфата натрия термодинамическая вероятность протекания реакции (3) становится выше реакции (4) при температурных интервалах ниже 550 °C;
– для сульфата лития условия первостепенной очередности протекания реакции (3), чем (4) соблюдается при температурных интервалах ниже 650 °C.
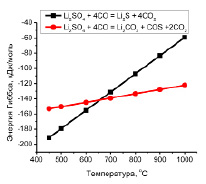
Рис. 4. Зависимость величины свободной энергии Гиббса от температуры для реакций восстановления сульфата лития монооксидом углерода
Таким образом, на основании проведенного термодинамического анализа можно заключить, что при низкотемпературном (450–650 °C) восстановлении сульфатов щелочных металлов монооксидом углерода (CO) образуется жидкая смесь, состоящая из карбонатов щелочных металлов с выделением газообразного карбонилсульфида (COS).
На рис. 5 показаны результаты лабораторных опытов по изучению очистки серосодержащих отходящих газов от вредных выбросов карбонатными расплавами щелочных металлов. На рис. 5 (A) видно, что после добавления летучей золы в карбонатный расплав и выдержки в течение 10 часов в EDS спектре полученного расплава отсутствуют пики, относящиеся к компонентам золы (Al2O3, SiO2, Fe2O3, CaO, MgO). Это указывает на незначительную растворимость составляющих летучей золы в смеси карбонатных солей щелочных металлов. На рис. 5 (Б) видно, что зола оседает в расплаве. По предлагаемой технологии осевшая зола легко может быть отделена от расплава отстаиванием и фильтрацией.
Результатами экспериментальных исследований установлено, что при взаимодействии серосодержащих компонентов отходящих газов с карбонатным расплавом щелочных металлов до 95 % серы поглощается расплавом.
На рис. 6 показаны результаты химической регенерации карбонатно-сульфатного расплава, полученного после глубокой очистки отходящих газов от серы монооксидом углерода. Нетрудно видеть, что EDS спектры проб (рис. 6 (A)), полученных после химической регенерации сульфатно-карбонатного расплава монооксидом углерода, не содержат линии серы, что свидетельствует о высокой степени извлечения серы. EDS cпектры полученных кристаллов подтверждают выделение элементарной серы, как продукта очистки отходящих газов (рис. 6 (Б), (B)).
Установлено, что при регенерации сульфатно-карбонатного расплава монооксидом углерода до 99 % серы извлекается из расплава в форме карбонилсульфида COS, наиболее удобной для получения товарной серной кислоты или элементарной серы.
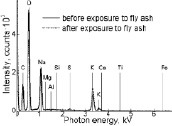

A Б
Рис. 5. EDS спектры Li-Na-K эвтектики до и после взаимодействия с золой отходящих газов (A) и фотография закристаллизованного расплава после взаимодействия с золой (Б). Темный слой в донной части образца (Б) соответствует осевшей пыли
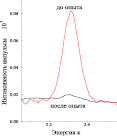

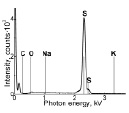
A Б B
Рис. 6. Результаты опытов по химической регенерации солевого расплава по химической регенерации карбонатно-сульфатного расплава. (A) – EDS спектры солевого расплава до и после обработки CO при 550 °C. Начальное содержание серы в расплаве 0,68 mM. Пик в области спектра с энергиями 2,2–2,4 eV соответствует сере. (Б) – Фотография кристаллов серы. Ширина снимка 1 мм. (B) – EDS спектр кристаллов серы, осажденной из расплава. Материал рекристаллизован перед анализом при 130 °C
В настоящее время с целью апробации новой технологии активно ведутся научно-исследовательские и опытно-промышленные испытания на угольной тепловой станции К-19 АО «3-Энергоорталык». Проведение запланированных работ в условиях максимального приближения к промышленному объекту делает предлагаемую инновационную технологию не только коммерчески привлекательной, но и экономически высокоэффективной и безопасной.
Сложившаяся тесная кооперация и проводимые совместные работы ученых КазНИТУ им. К.И. Сатпаева, Научного института имени Вейцмана (Израиль) и инженерно-технических работников АО «3-Энергоорталык» вселяют уверенность, что внедрение принципиально новой технологии высокоэффективной и экономичной санитарной очистки серосодержащих газов ТЭЦ, применимой как в условиях Казахстана, так и за рубежом, будет вполне успешным.
Выводы
1. Представлены теоретические основы новой технологии глубокой очистки отходящих газов тепловых электростанций расплавами карбонатов щелочных металлов с получением товарных вторичных продуктов. Применение разработанной технологии позволит значительно сократить выбросы серы (до 0,001 %) и золы топливными электростанциями и металлургическими заводами Республики Казахстан без образования дополнительных твердых или жидких отходов и без использования дорогостоящих материалов и реагентов.
2. Снижение эмиссий вредных веществ в окружающую среду позволит стабилизировать и улучшить качество окружающей среды и восстановить баланс природной среды.
3. Применение технологии позволит вовлечь на переработку более дешевые серосодержащие угли для производства электроэнергии, что обеспечит большой экономический эффект действующим предприятиям. К примеру, в США цена угля с высоким содержанием серы (5 %) составляет 60 % от цены угля с низким содержанием серы. При этом снижение затрат на производство электроэнергии с учетом стоимости очистки отходящих газов составляет около 30 %.
4. Разработанная технология глубокой очистки газов без особых затрат легко может быть интегрирована в существующую инфраструктуру действующих ТЭЦ и металлургических предприятий.



