Гидроксилсодержащие соединения и их производные находят широкое применение в различных областях химии (полимерная, органическая, синтетическая, фармакологическая химия и др.). Во многих случаях именно наличие гидроксильной функции придает органическим соединениям желаемые свойства (например, антимикробное или противопаразитарное действие спиртов и фенолов) или делает возможным получение целевого продукта (например, синтез биополимеров и некоторых синтетический полимеров реакцией поликонденсации).
Однако в некоторых случаях наличие гидроксильной группы является нежелательным (например, придает значительные местнораздражающие свойства терапевтическим препаратам). Поэтому поиск новых методов модификации гидроксилсодержащих соединений является актуальным.
Одним из распространенных методов трансформации гидроксильной функции является ее алкилирование с помощью различных реагентов (алкилгалогениды, непредельные соединения, спирты, эфиры серной и сульфокислот), что приводит к получению простых или сложных эфиров. Однако, применение этих реагентов не всегда представляется возможным из-за присутствия в субстрате функциональных групп.
На наш взгляд, перспективным направлением такой модификации является алкилирование с помощью различных производных би- и трициклических систем, которые кроме нивелирования указанных нежелательных свойств придадут терапевтическим препаратам дополнительную липофильность, что во многих случаях является полезным.
Перспективным адамантилирующим агентом является представитель класса напряженных пропелланов – 1,3-дегидроадамантан (ДГА), который чрезвычайно реакционноспособен в реакциях с протоноподвижными соединениями. В литературе описаны способы адамантилирования гидроксилсодержащих соединений с помощью 1,3-ДГА, таких как фенол и его производные, нафтол [1-3]. По аналогичной методике была проведена реакция адамантилирования 7-гидрокси-4-метилкумарина, в котором наряду с фенольным фрагментом содержится остаток α-пирона:
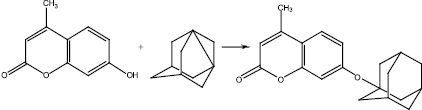
Реакцию 1,3-ДГА с 7-гидрокси-4-метилкумарином осуществлялась при мольном соотношении реагентов 1:1 в осушенном инертном растворителе – диэтиловом эфире при температуре 30-35 ºС в атмосфере сухого аргона, в течение 0,5 ч.
Анализ продуктов реакции методом хромато-масс-спектроскопии показал, что основным направлением реакции является селективное О-алкилирование ДГА с образованием адамант-1-илового эфира c выходом до 95 %. Особенностью этой реакции является отсутствие продуктов адамантилирования ароматического кольца, в отличие от реакций с участием фенолов и нафтолов [1,3]. Состав и строение полученных продуктов были подтверждены методами ЯМР 1Н-спектроскопии и хромато-масс-спектрометрии.



