Scientific journal
Modern high technologies
ISSN 1812-7320
"Перечень" ВАК
ИФ РИНЦ = 1,279
APPLICATION OF THEORETICAL MODEL OF CARRY OF ENERGY IN SPIRITS SOLUTIONS OF I-I ELECTROLYTES AND THEIR EXPERIMENTAL ESTIMATION
Для совершенствования и оптимизации технологических процессов необходимы научно обоснованные инженерные расчеты, которые нуждаются в информации о теплофизических и термодинамических свойствах рабочего вещества в широкой области изменения температур и концентраций. Использование ориентировочных или даже приближенных данных по свойствам веществ в инженерных расчетах приводит к существенному завышению металлоемкости установок и снижению их технико-экономических показателей.
В связи с этим, дальнейшее уточнение теплофизических данных рабочих веществ представляет собой значительный резерв совершенствования технологического процесса.
Разработан целый ряд новых технологических процессов, протекающих при высоких температурах, что послужило основанием для совершенствования и интенсификации ранее существующих процессов, применяемых в химической, нефтехимической, топливной, нефтеперерабатывающей промышленности с крупнотоннажным производством [3,4].
Известные модельные представления теплопроводности растворов электролитов не приемлемы при оценке переноса количества энергии в неводных, в частности спиртовых, растворах электролитов.
В ходе исследований предполагается
применить теоретическую модель теплопроводности в спиртовых растворах
I-I электролитов и их экспериментальная оценка.
Теоретическая оценка теплопроводности проводилась по уравнению плазмоподобной теории электролитов, разработанной для водных растворов электролитов и предполагающей привлечение индивидуальных свойств отдельных ионов и их коллективных эффектов, таких как плазменная частота, дебаевский радиус, подвижность ионов, сольватные числа, радиусы сольватированных ионов, массы сольватированных ионов в неводных растворах [1,5]. Также применение данной модели для расчета теплопроводности предполагает использование диэлектрической постоянной, энергии межмолекулярных взаимодействий, дипольного момента, радиуса и молярной массы молекулы растворителя. В общем виде уравнение для определения коэффициента теплопроводности имеет вид [1,2,5]:
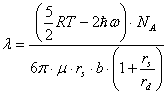 ,
,
где R-
газовая постоянная; T-
температура, К; ![]() - энергия колебательного процесса ²ассоциация - диссоциация²; zie-
элементарный заряд;
- энергия колебательного процесса ²ассоциация - диссоциация²; zie-
элементарный заряд; ![]() - постоянная Планка; C - концентрация раствора, моль/л; NA-
постоянная Авогадро;
- постоянная Планка; C - концентрация раствора, моль/л; NA-
постоянная Авогадро; ![]() - приведенная масса несольватированных
ионов; mi-
молярная масса иона;
- приведенная масса несольватированных
ионов; mi-
молярная масса иона; 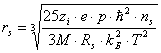 - радиус сольватированных ионов; p - дипольный момент молекулы
растворителя;
- радиус сольватированных ионов; p - дипольный момент молекулы
растворителя; ![]() - сольватное число иона; RS - радиус молекулы растворителя; ri-
радиус иона; kБ- постоянная
Больцмана; ε - диэлектрическая постоянная; M - молярная масса растворителя;
- сольватное число иона; RS - радиус молекулы растворителя; ri-
радиус иона; kБ- постоянная
Больцмана; ε - диэлектрическая постоянная; M - молярная масса растворителя; ![]() - подвижность иона; ΔH - энергия водородной связи
растворителя;
- подвижность иона; ΔH - энергия водородной связи
растворителя; 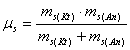 - приведенная масса
сольватированных ионов; ms=m+ns·M -
масса сольватированного иона;
- приведенная масса
сольватированных ионов; ms=m+ns·M -
масса сольватированного иона; 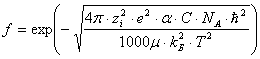 - функция максвелловского распределения
по скоростям движения ионов;
- функция максвелловского распределения
по скоростям движения ионов;
α - степень диссоциации электролита; 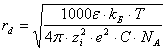 - дебаевский радиус экранирования
[1].
- дебаевский радиус экранирования
[1].
В табл. 1 представлены значения теплопроводности электролитов I-I (Kl, NaBr, NH4Cl) в среде метанола и пропанола, полученные по рассматриваемой теоретической модели.
Экспериментальную оценку теплопроводности спиртовых растворов электролитов I-I проводили на установке, апробированной на водных растворах электролитов [6].
Установка для определения теплопроводности растворов электролитов содержит электрически связанные два датчика-преобразователя, блок регистрации, источник питания. Термоэлектроды располагаются внутри датчиков-преобразова-телей, которые соединяются с регистрирующим блоком. При этом один из датчиков соединяется с источником питания и помещается в термостатированную измерительную ячейку с исследуемым раствором, поддерживающую постоянную температуру с помощью жидкостного термостата, а другой датчик помещается в микрохолодильник с тающим льдом [6].
В табл. 2, 3 представлены расчетные и экспериментальные значения теплопроводности электролитов I-I в среде этанола и бутанола.
На рис. 1, 2 представлена зависимость теплопроводности некоторых спиртовых растворов электролитов I-I от температуры и концентрации.
Показано, что теплопроводность исследуемых объектов увеличивается с ростом температуры и уменьшается с ростом концентрации.
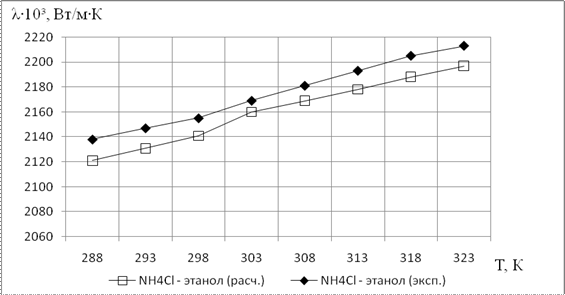
Рис. 1. Температурная зависимость
теплопроводности NH4Clв среде этанола при C=0,1 моль/л
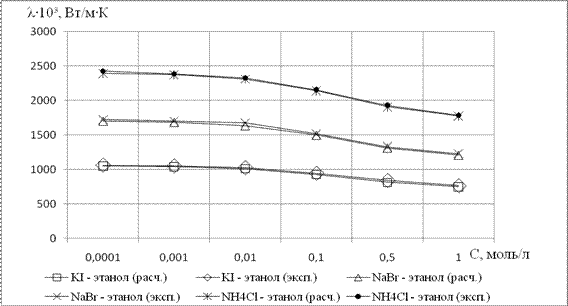
Рис. 2. Концентрационная зависимость теплопроводности электролитов I-I (Kl, NaBr, NH4Cl) в среде этанола
Экспериментальная установка обладает достаточной воспроизводимостью получаемых данных по теплопроводности водных растворов электролитов и может использоваться для определения теплопроводности спиртовых растворов электролитов в интервале концентраций и температур.
Примененный комплекс расчетных методов для оценки теплопроводности растворов электролитов в диапазоне температур и концентраций дает удовлетворительные данные в таких растворителях как метанол, этанол, пропанол, бутанол. Пользуясь теоретической моделью, учитывающей характеристики растворителя, возможно получение данных по теплопроводности растворов электролитов в неводных растворителях.
Изучение теплофизических и термодинамических свойств растворов в значительной степени способствует развитию и совершенствованию современной теории жидкого состояния, выяснению механизма межмолекулярного взаимодействия в жидкостях. Поэтому результаты исследования теплопроводности легли в основу современной молекулярно-кинетической теории жидкостей.
Таблица 1
Расчетные значения теплопроводности электролитов I-I
(KI,
NaBr, NH4Cl
)
в среде метанола и пропанола
|
λ·103, Вт/м·К |
||||||||
|
C, моль/л
|
T,K |
|||||||
|
288 |
293 |
298 |
303 |
308 |
313 |
318 |
323 |
|
|
KI - метанол |
||||||||
|
1 |
340 |
343 |
346 |
351 |
353 |
356 |
359 |
362 |
|
0.5 |
367 |
370 |
373 |
378 |
380 |
383 |
386 |
388 |
|
0.1 |
415 |
418 |
420 |
424 |
426 |
428 |
431 |
433 |
|
0.01 |
450 |
452 |
453 |
457 |
459 |
460 |
462 |
464 |
|
0.001 |
462 |
464 |
465 |
469 |
470 |
472 |
473 |
475 |
|
0.0001 |
466 |
468 |
470 |
472 |
474 |
475 |
477 |
478 |
|
NaBr - метанол |
||||||||
|
1 |
532 |
536 |
541 |
548 |
552 |
556 |
561 |
565 |
|
0.5 |
575 |
579 |
583 |
590 |
594 |
598 |
602 |
606 |
|
0.1 |
650 |
654 |
657 |
663 |
666 |
670 |
673 |
676 |
|
0.01 |
705 |
708 |
710 |
716 |
718 |
721 |
723 |
725 |
|
0.001 |
725 |
727 |
730 |
735 |
737 |
739 |
741 |
743 |
|
0.0001 |
732 |
734 |
736 |
741 |
743 |
745 |
747 |
749 |
|
NH4Cl - матанол |
||||||||
|
1 |
751 |
757 |
762 |
772 |
776 |
781 |
787 |
792 |
|
0.5 |
803 |
809 |
814 |
823 |
827 |
832 |
837 |
842 |
|
0.1 |
894 |
898 |
902 |
910 |
913 |
917 |
921 |
925 |
|
0.01 |
959 |
962 |
965 |
971 |
974 |
977 |
980 |
982 |
|
0.001 |
982 |
984 |
987 |
993 |
996 |
998 |
1000 |
1003 |
|
0.0001 |
990 |
992 |
994 |
1001 |
1003 |
1005 |
1007 |
1009 |
|
KI -пропанол |
||||||||
|
1 |
1433 |
1446 |
1459 |
1478 |
1489 |
1501 |
1513 |
1525 |
|
0.5 |
1568 |
1581 |
1593 |
1611 |
1622 |
1633 |
1644 |
1655 |
|
0.1 |
1810 |
1820 |
1829 |
1846 |
1855 |
1864 |
1872 |
1882 |
|
0.01 |
1988 |
1996 |
2003 |
2017 |
2024 |
2031 |
2037 |
2044 |
|
0.001 |
2054 |
2060 |
2066 |
2080 |
2085 |
2019 |
2097 |
2102 |
|
0.0001 |
2076 |
2082 |
2087 |
2101 |
2106 |
2111 |
2116 |
2122 |
|
NaBr - пропанол |
||||||||
|
1 |
2357 |
2378 |
2399 |
2431 |
2448 |
2468 |
2487 |
2506 |
|
0.5 |
2578 |
2598 |
2617 |
2648 |
2665 |
2683 |
2701 |
2719 |
|
0.1 |
2977 |
2993 |
3008 |
3036 |
3050 |
3065 |
3079 |
3093 |
|
0.01 |
3277 |
3288 |
3300 |
3324 |
3334 |
3345 |
3355 |
3366 |
|
0.001 |
3388 |
3398 |
3408 |
3430 |
3439 |
3448 |
3457 |
3465 |
|
0.0001 |
3426 |
3435 |
3443 |
3465 |
3474 |
3482 |
3490 |
3498 |
|
NH4Cl - пропанол |
||||||||
|
1 |
3546 |
3575 |
3604 |
3651 |
3673 |
3701 |
3727 |
3754 |
|
0.5 |
3839 |
3866 |
3893 |
3938 |
3959 |
3985 |
4009 |
4034 |
|
0.1 |
4357 |
4379 |
4401 |
4440 |
4459 |
4479 |
4499 |
4518 |
|
0.01 |
4742 |
4758 |
4773 |
4807 |
4822 |
4837 |
4851 |
4865 |
|
0.001 |
4884 |
4897 |
4910 |
4942 |
4954 |
4967 |
4979 |
4991 |
|
0.0001 |
4931 |
4943 |
4956 |
4986 |
4998 |
5010 |
5021 |
5033 |
Таблица 2
Расчетные и экспериментальные значения теплопроводности электролитов I-I (KL, NaBr, NH4Cl ) в среде этанола
|
T,K |
C, моль/л |
KI |
NaBr |
NH4Cl |
|||
|
λрасч.*103 |
λэксп.*103 | λрасч.*103 |
λэксп.*103 |
λрасч.*103 |
λэксп.*103 |
||
|
288 |
1 |
734 |
745 |
1185 |
1199 |
1745 |
1761 |
|
0.5 |
800 |
817 |
1291 |
1306 |
1881 |
1899 |
|
|
0.1 |
916 |
933 |
1480 |
1496 |
2121 |
2138 |
|
|
0.01 |
1002 |
1010 |
1620 |
1643 |
2296 |
2307 |
|
|
0.001 |
1033 |
1039 |
1672 |
1689 |
2360 |
2357 |
|
|
0.0001 |
1043 |
1051 |
1690 |
1704 |
2381 |
2395 |
|
|
293 |
1 |
740 |
756 |
1195 |
1210 |
1759 |
1773 |
|
0.5 |
806 |
822 |
1301 |
1314 |
1894 |
1911 |
|
|
0.1 |
921 |
939 |
1488 |
1504 |
2131 |
2147 |
|
|
0.01 |
1005 |
1018 |
1626 |
1651 |
2303 |
2316 |
|
|
0.001 |
1036 |
1045 |
1677 |
1694 |
2366 |
2378 |
|
|
0.0001 |
1046 |
1057 |
1694 |
1710 |
2387 |
2409 |
|
|
298 |
1 |
747 |
763 |
1206 |
1224 |
1773 |
1785 |
|
0.5 |
812 |
839 |
1310 |
1325 |
1907 |
1929 |
|
|
0.1 |
926 |
944 |
1495 |
1512 |
2141 |
2155 |
|
|
0.01 |
1009 |
1025 |
1632 |
1669 |
2311 |
2326 |
|
|
0.001 |
1039 |
1050 |
1682 |
1701 |
2373 |
2388 |
|
|
0.0001 |
1049 |
1062 |
1699 |
1722 |
2393 |
2426 |
|
|
303 |
1 |
757 |
771 |
1222 |
1240 |
1795 |
1797 |
|
0.5 |
822 |
845 |
1326 |
1337 |
1929 |
1941 |
|
|
0.1 |
935 |
951 |
1509 |
1521 |
2160 |
2169 |
|
|
0.01 |
1016 |
1029 |
1644 |
1677 |
2327 |
2336 |
|
|
0.001 |
1046 |
1057 |
1693 |
1712 |
2388 |
2395 |
|
|
0.0001 |
1056 |
1068 |
1709 |
1738 |
2408 |
2434 |
|
|
308 |
1 |
762 |
788 |
1230 |
1254 |
1806 |
1813 |
|
0.5 |
827 |
852 |
1334 |
1349 |
1939 |
1954 |
|
|
0.1 |
939 |
956 |
1516 |
1533 |
2169 |
2181 |
|
|
0.01 |
1020 |
1033 |
1649 |
1681 |
2334 |
2358 |
|
|
0.001 |
1049 |
1061 |
1697 |
1724 |
2394 |
2409 |
|
|
0.0001 |
1059 |
1073 |
1714 |
1746 |
2413 |
2442 |
|
|
313 |
1 |
769 |
797 |
1240 |
1263 |
1819 |
1825 |
|
0.5 |
833 |
867 |
1343 |
1361 |
1951 |
1968 |
|
|
0.1 |
944 |
961 |
1523 |
1541 |
2178 |
2193 |
|
|
0.01 |
1023 |
1039 |
1654 |
1689 |
2341 |
2365 |
|
|
0.001 |
1052 |
1064 |
1702 |
1733 |
2400 |
2418 |
|
|
0.0001 |
1062 |
1078 |
1718 |
1751 |
2419 |
2449 |
|
|
318 |
1 |
775 |
802 |
1249 |
1275 |
1832 |
1846 |
|
0.5 |
839 |
872 |
1352 |
1376 |
1963 |
1971 |
|
|
0.1 |
949 |
968 |
1530 |
1549 |
2188 |
2205 |
|
|
0.01 |
1027 |
1043 |
1660 |
1696 |
2348 |
2372 |
|
|
0.001 |
1055 |
1069 |
1706 |
1745 |
2405 |
2429 |
|
|
0.0001 |
1064 |
1082 |
1722 |
1758 |
2424 |
2451 |
|
|
323 |
1 |
781 |
814 |
1259 |
1283 |
1844 |
1854 |
|
0.5 |
844 |
879 |
1361 |
1385 |
1974 |
1985 |
|
|
0.1 |
953 |
973 |
1537 |
1557 |
2197 |
2213 |
|
|
0.01 |
1030 |
1047 |
1665 |
1700 |
2354 |
2380 |
|
|
0.001 |
1058 |
1075 |
1711 |
1751 |
2411 |
2437 |
|
|
0.0001 |
1067 |
1090 |
1726 |
1764 |
2430 |
2459 |
|
Таблица 3
Расчетные и экспериментальные значения теплопроводности электролитов I-I (KI, NABr, NH4Cl) в среде бутанола
|
T,K |
C, моль/л |
KI |
NaBr |
NH4Cl |
|||
|
λрасч*103 |
λэксп*103 |
λрасч*103 |
λэксп*103 |
λрасч*103 |
λэксп*103 |
||
|
288 |
1 |
1060 |
1099 |
3699 |
3711 |
5619 |
5600 |
|
0.5 |
1188 |
1202 |
4054 |
4031 |
6095 |
6058 |
|
|
0.1 |
1436 |
1449 |
4699 |
4687 |
6949 |
6925 |
|
|
0.01 |
1634 |
1647 |
5188 |
5149 |
7580 |
7561 |
|
|
0.001 |
1711 |
1725 |
5371 |
5358 |
7815 |
7796 |
|
|
0.0001 |
1737 |
1747 |
5432 |
5408 |
7894 |
7877 |
|
|
293 |
1 |
1071 |
1117 |
3732 |
3721 |
5666 |
5623 |
|
0.5 |
1200 |
1213 |
4085 |
4060 |
6139 |
6093 |
|
|
0.1 |
1445 |
1458 |
4724 |
4701 |
6981 |
6947 |
|
|
0.01 |
1641 |
1658 |
5206 |
5177 |
7606 |
7590 |
|
|
0.001 |
1716 |
1733 |
5386 |
5364 |
7837 |
7809 |
|
|
0.0001 |
1742 |
1752 |
5446 |
5423 |
7914 |
7898 |
|
|
298 |
1 |
1082 |
1131 |
3765 |
3743 |
5712 |
5687 |
|
0.5 |
1210 |
1227 |
4116 |
4086 |
6183 |
6137 |
|
|
0.1 |
1454 |
1470 |
4749 |
4721 |
7016 |
6993 |
|
|
0.01 |
1647 |
1665 |
5225 |
5201 |
7632 |
7603 |
|
|
0.001 |
1722 |
1740 |
5401 |
5389 |
7859 |
7825 |
|
|
0.0001 |
1747 |
1765 |
5460 |
5430 |
7934 |
7906 |
|
|
303 |
1 |
1093 |
1140 |
3816 |
3781 |
5787 |
5712 |
|
0.5 |
1221 |
1239 |
4165 |
4127 |
6255 |
6189 |
|
|
0.1 |
1463 |
1485 |
4794 |
4749 |
7080 |
7030 |
|
|
0.01 |
1654 |
1673 |
5263 |
5229 |
7687 |
7638 |
|
|
0.001 |
1727 |
1748 |
5436 |
5411 |
7909 |
7874 |
|
|
0.0001 |
1751 |
1777 |
5494 |
5452 |
7984 |
7931 |
|
|
308 |
1 |
1104 |
1152 |
3843 |
3800 |
5823 |
5739 |
|
0.5 |
1232 |
1245 |
4192 |
4145 |
6290 |
6230 |
|
|
0.1 |
1472 |
1499 |
4816 |
4780 |
7110 |
7085 |
|
|
0.01 |
1660 |
1681 |
5279 |
5247 |
7710 |
7683 |
|
|
0.001 |
1732 |
1752 |
5451 |
5420 |
7930 |
7901 |
|
|
0.0001 |
1756 |
1782 |
5508 |
5477 |
8003 |
7972 |
|
|
313 |
1 |
1115 |
1156 |
3874 |
3837 |
5867 |
5794 |
|
0.5 |
1242 |
1257 |
4221 |
4189 |
6331 |
6291 |
|
|
0.1 |
1481 |
1506 |
4839 |
4800 |
7143 |
7115 |
|
|
0.01 |
1667 |
1690 |
5297 |
5260 |
7734 |
7702 |
|
|
0.001 |
1737 |
1760 |
5465 |
5433 |
7950 |
7914 |
|
|
0.0001 |
1761 |
1788 |
5521 |
5498 |
8022 |
8001 |
|
|
318 |
1 |
1125 |
1161 |
3904 |
3876 |
5910 |
5831 |
|
0.5 |
1252 |
1269 |
4250 |
4205 |
6371 |
6322 |
|
|
0.1 |
1489 |
1519 |
4862 |
4827 |
7175 |
7142 |
|
|
0.01 |
1673 |
1698 |
5313 |
5294 |
7758 |
7721 |
|
|
0.001 |
1742 |
1768 |
5479 |
5445 |
7970 |
7932 |
|
|
0.0001 |
1766 |
1792 |
5534 |
5507 |
8041 |
8020 |
|
|
323 |
1 |
1136 |
1165 |
3934 |
3901 |
5953 |
5878 |
|
0.5 |
1262 |
1282 |
4278 |
4233 |
6411 |
6388 |
|
|
0.1 |
1497 |
1525 |
4885 |
4851 |
7206 |
7193 |
|
|
0.01 |
1679 |
1702 |
5330 |
5309 |
7781 |
7744 |
|
|
0.001 |
1747 |
1773 |
5493 |
5460 |
7990 |
7969 |
|
|
0.0001 |
1770 |
1796 |
5547 |
5518 |
8059 |
8031 |
|
СПИСОК ЛИТЕРАТУРЫ:
1. Багаева Т.В., Бубеева И.А. // Молодые исследователи - регионам.-2008.-Т.1.-С. 4.
2. Балданов М.М., Танганов Б.Б., Бубеева И.А. // Докл. СО АН ВШ. 2003. № 2(8). С. 14.
3. Бубеева И.А. Разработка теоретической модели оценки коэффициента теплопроводности в рамках плазмоподобной концепции растворов электролитов: Автореф. дис. ... канд. техн. наук.- Улан-Удэ: - 2004. - 22 с.
4. Зарипова М.А. Теплофизические и термодинамические свойства водных растворов гидразина и фенилгидразина: Автореф. дис. ... канд. техн. наук.- Душанбе: - 2006. - 19 с.
5. Танганов Б.Б., Бубеева И.А., Багатева Т.В. // Наука и образование - 2008. -[Электр. ресурс] / МГТУ. Электр. текст дан. (20 Мб). Мурманск: МГТУ, 2008. 1 опт. компакт - диск (CD-ROM).
6. Патент на полезную модель № 34250, МПК G01N25/18. Установка для определения теплопроводности растворов электролитов / Б.Б. Танганов, В.Ч.-Д. Гармаев, И.А. Бубеева, Ж.В. Гармаев.- Заяв. 23.06.2003; Опубл. 27.11.2003, Бюл. № 33.
Библиографическая ссылка
Багаева Т.В., Танганов Б.Б., Бубеева И.А. ПРИМЕНЕНИЕ ТЕОРЕТИЧЕСКОЙ МОДЕЛИ ПЕРЕНОСА ЭНЕРГИИ В СПИРТОВЫХ РАСТВОРАХ I-I ЭЛЕКТРОЛИТОВ И ИХ ЭКСПЕРИМЕНТАЛЬНАЯ ОЦЕНКА // Современные наукоемкие технологии. 2009. № 12. С. 8-14;URL: https://top-technologies.ru/en/article/view?id=25874 (дата обращения: 16.05.2026).



