Scientific journal
Modern high technologies
ISSN 1812-7320
"Перечень" ВАК
ИФ РИНЦ = 1,279
ON THE ROLE OF THE ACTIVATION OF LYPOPEROXIDATION IN THE MECHANISMS OF ISCHEMIC DAMAGE OF MYOCARDIUM
В то же время активация свободнорадикального окисления является типовым процессом дестабилизации биологических мембран при гипоксии, ишемии, стрессовых ситуациях, эндокринопатиях, различных бактериальных инфекциях и интоксикациях [2,7].
Чрезмерная активация свободнорадикального окисления и перекисных реакций - важнейший патогенетический фактор дезорганизации структурных и ферментных белков биологических мембран, повышения их пассивной проницаемости по осмотическому градиенту при одновременном подавлении активности энергозависимого транспорта молекул органических и неорганических соединений. Изменение трансмембранного переноса ионов при интенсификации липопероксидации, безусловно, приводит к нарушению процессов деполяризации, реполяризации клеток и их возбудимости [7].
Целью настоящего исследования явилось изучение динамики, а также корреляционной взаимосвязи интегративных показателей состояния процессов липопероксидации и антиоксидантной системы гомогенатов миокарда и крови в процессе развития острой ишемии миокарда.
Материалы и методы исследования. Эксперименты проведены на 60 беспородных крысах- самцах массой 250-300 г. Моделирование ишемии и инфаркта миокарда проводили в условиях острого опыта по методу Н.Selye (окклюзия нисходящей ветви левой коронарной артерии на уровне нижнего края ушка) [9]. Одновременно проводили морфологическую и гистохимическую оценку состояния миокарда.
Динамику структурных изменений миокарда сопоставляли с интенсивностью процессов липопероксидации и состоянием антиоксидантной системы гомогенатов миокарда и крови.
О состоянии антиоксидантной системы судили по уровню активности супероксиддисмутазы (СОД) [1], каталазы [3], а также по уровню восстановленного глутатиона [1,4] крови и гомогенатов миокарда. Об интенсивности процессов липопероксидации свидетельствовала динамика содержания диеновых конъюгатов (ДК) [8] и малонового диальдегида (МДА) [6] в крови и гомогенатах миокарда на фоне развития острой ишемии миокарда.
Результаты исследований и их обсуждение. Как показали результаты проведенных нами исследований, спустя 60 мин. с момента развития ишемии имело место резкое возрастание уровня МДА (р<0.001, рис. 1) в миокарде.
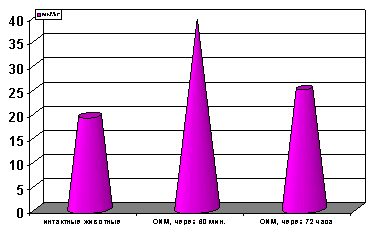
Рисунок 1. Содержание МДА гомогенатов миокарда в условиях острой ишемии миокарда.
Примечание: ОИМ - острая ишемия миокарда через 60 мин. и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в текстах.
Одновременно отмечалось и увеличение содержания МДА (р<0.001, рис.2) в сыворотке крови.
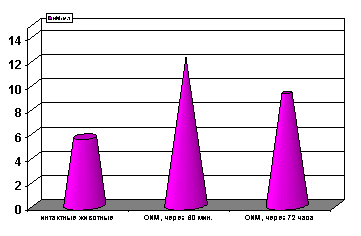
Рисунок 2. Содержание МДА сыворотки крови в условиях острой ишемии миокарда.
Примечание: ОИМ - острая ишемия миокарда через 60 мин. и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в текстах.
При этом уровень ДК (р<0.001, рис. 3) в крови не отличался от показателей группы контрольных интактных животных.
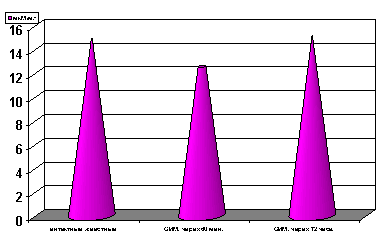
Рисунок 3. Содержание диеновых конъюгатов сыворотки крови в условиях острой ишемии миокарда.
Примечание: ОИМ - острая ишемия миокарда через 60 мин. и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в текстах.
Спустя 72 часа с момента развития ишемии уровень МДА (р<0.001, рис.1) в миокарде несколько снижался по сравнению с таковыми показателями в предшествующий период наблюдения (60 мин с момента развития ишемии), но в то же время оставался выше показателей группы интактных контрольных животных. Содержание МДА (р<0.001, рис.2) в сыворотке крови спустя 72 часа с момента развития ишемии также оставалось значительно выше показателей контроля, но в то же время несколько снижалось по сравнению с ранним периодом острой ишемии миокарда. Уровень ДК (р<0.001, рис. 3) в крови оставался без изменений в течение всего периода наблюдений.
Таким образом, выявление параллелизма между уровнем МДА миокарде и сыворотке крови в динамике острой ишемии миокарда свидетельствует о том, что показатель содержания МДА в крови может быть одним из объективных критериев оценки развития ишемии миокарда, наряду с общепринятыми показателями тестированиями инфаркта миокарда по уровню трансаминаз сыворотки крови. Содержание ДК в крови при ишемии миокарда практически не изменяется и не может быть использовано для оценки степени структурных изменений в ишемизированном миокарде.
Одним из патогенетических факторов активации процессов липопероксидации в условиях ишемии может явиться недостаточность антиоксидантной системы крови и тканей. Для частичного решения этого вопроса проведены сравнительные серии экспериментов по установлению корреляционной взаимосвязи состояний активности СОД, каталазы, восстановленного глутатиона крови и гомогенатов миокарда в динамике острой ишемии.
Использование указанного комплекса показателей антиоксидантной защиты клеток не является случайным. Как известно, в условиях нормы молекулярный кислород подвергается тетравалентному восстановлению в митохондриях, в биологическом процессе, связанном с генерацией АТФ (Ерюхин И.Л., Шляпников С.А.,1997). В условиях ишемии миокарда активизируются процессы одно - и трехэлектронного восстановления кислорода. В этом процессе молекулярный кислород восстанавливается сначала в супероксидный анион-радикал, который затем может превратиться в перекись водорода. Последующее одновалентное восстановление перекиси водорода приводит к образованию чрезвычайно реактогенного гидроксильного радикала. В цитозоле клеток супероксидный анион-радикал генерируется при участии ксантиноксидазы [2,7].
Как известно, при гипоксиях различного генеза усиливается трансформация ксантиндегидрогеназы в ксантиноксидазу (Рашби Э.Ю., Варштанян Л.С., Серегина Л.А.,1986).Таким образом, выявленная нами закономерность избыточного накопления МДА в гомогенатах миокарда, сыворотки крови и ДК сыворотки крови в динамике развития острой ишемии миокарда может быть следствием абсолютной или относительной недостаточности активности супероксиддисмутазы, каталазы или повышения активности ксантиноксидазы.
Установлено, что СОД ускоряет спонтанную дисмутацию супероксидного анион-радикала примерно в 20 раз. Образующаяся в процессе дисмутации супероксидного анион-радикала перекись водорода восстанавливается до воды, в основном, каталазой и глутатионпероксидазой. Важная роль в антиоксидантной защите организма отводится SH-соединениям - активным перехватчикам гидроксильных радикалов, в частности, восстановленному глутатиону [5].
Выше изложенное и определило целесообразность исследования активности СОД, каталазы и уровня восстановленного глутатиона в гомогенатах миокарда и в крови.
Как показали результаты проведенных экспериментов, спустя 60 мин. с момента развития ишемии отмечалось снижение активности СОД (р<0.001, рис. 4) гомогенатов миокарда, между тем активность СОД (р<0.001, рис. 5) сыворотки крови возрастала по сравнению с таковыми показателями группы контроля.
Спустя 72 часа с момента развития ишемии активность СОД (р<0.001, рис. 4) гомогенатов миокарда оставалась сниженной, как и в предыдущей группе наблюдения. Одновременно резко снижалась активность СОД (р<0.001, рис. 5) сыворотки крови как по сравнению с таковыми показателями группы животных с ранней стадией острой гипоксии, так и по отношению к показателям контрольной группы животных.
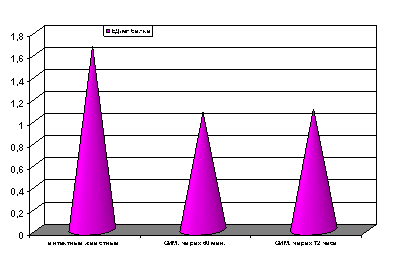
Рисунок 4. Содержание СОД гомогенов миокарда в условиях острой ишемии миокарда.
Примечание: ОИМ - острая ишемия миокарда через 60 мин. и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в текстах.
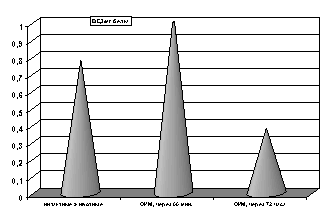
Рисунок 5. Содержание СОД сыворотки крови в условиях острой ишемии миокарда.
Примечание: ОИМ - острая ишемия миокарда через 60 мин. и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в текстах.
Касаясь выявленного нами феномена разнонаправленных изменений активности СОД гомогенатов миокарда и сыворотки крови в ранние сроки ишемии миокарда, следует остановиться на различиях происхождения и структуры изучаемого фермента. В настоящее время обнаружено несколько изоэнзимных форм СОД, отличающихся строением активного центра. У эукариотов Cu-, Zn-содержащая СОД локализуется в основном в цитозоле эритроцитов, а в митохондриях миокарда локализована Mn- содержащая СОД. Указанные ферменты проявляют активность внутриклеточно, а в межклеточной жидкости быстро разрушаются (Фридович И., 1970, Поберезкина Н.Б., Осинская Л.Ф., 1989, Калия Е.С., Синько Н.М., 1991). Однако сыворотка крови также обладает активностью супероксиддисмутазы за счет наличия в ней высокомолекулярной формы СОД, хорошо связывающейся гепаринсульфатом гликокаликса эндотелиоцитов и защищающая их от свободных радикалов. В то же время гликопротеид сыворотки крови - церулоплазмин также обладает супероксиддисмутазной активностью [5,7].
Таким образом, различные изоферменты СОД обладают различной чувствительностью к действию гипоксического фактора. Активация СОД сыворотки крови на ранних этапах ишемии миокарда, безусловно, носит компенсаторный характер и препятствует развитию дезорганизации структуры мембран клеток крови, эндотелиоцитов, развитию эндотелиальной дисфункции. Однако и этот механизм адаптации к гипоксии истощается к 3 суткам развития ишемии миокарда.
Что касается активности другого фермента - каталазы в динамике ишемии миокарда, следует отметить стабильное снижение ее активности в ранние и поздние сроки наблюдения в гомогенатах миокарда (р<0.001, рис.6).
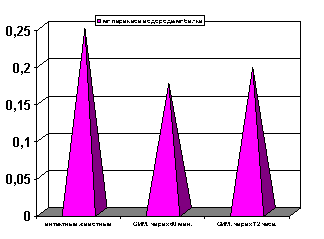
Рисунок 6. Содержание катализы гомогенов миокарда в условиях острой ишемии миокарда.
Примечание: ОИМ - острая ишемия миокарда через 60 мин. и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в текстах.
Как известно каталаза клеточного происхождения, локализуется в основном в пероксисомах, частично микросомах и в меньшей степени в цитозоле клеток.
Таким образом, выявленный нами факт параллельного снижения активности СОД и каталазы миокарда не является случайным, известно, что СОД и каталаза действуют как звенья антиоксидантной системы, обеспечивая переключение потока электронов с одной цепи транспорта на другую [5].
Проведенное нами определение активности каталазы в сыворотке крови в условиях нормы свидетельствовало о значительно более низком уровне ее активности по сравнению с внутриклеточным, что соответствует данным литературы (Петрович Ю.А., Гуткин Д.В., 1980, Дубинина Е.У., 1989, Поберезкина Н.Б., Осинская Л.Ф., 1998).Однако, в динамике острой ишемии миокарда отмечены фазные изменения активности этого фермента сыворотки крови (р<0.001, рис.7): возрастание активности на ранней стадии ишемии миокарда сменялось подавлением активности этого фермента на поздней стадии патологии.
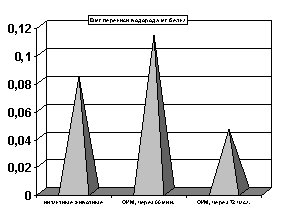
Рисунок 7. Содержание катализы сыворотки крови в условиях острой ишемии миокарда.
Примечание: ОИМ - острая ишемия миокарда через 60 мин. и 72 часа с момента развития ишемии миокарда. Степень достоверности полученных данных указаны в текстах.
Возрастание активности каталазы, спустя 60 мин с момента развития ишемии, по всей вероятности, является одним из проявлений синдрома цитолиза, когда внутриклеточные белки-ферменты за счет пассивной диффузии проникают через цитоплазматическую мембрану в системный кровоток.
Как известно, важнейшими компонентами антиоксидантной, антирадикальной защиты клеток является восстановленный глутатион, сравнительная оценка содержания которого в миокарде и сыворотке крови проведены нами в динамике острой ишемии миокарда.
Как показали результаты проведенных нами исследований, содержание восстановленого глутатиона в гомогенатах миокарда заметно снижалось уже спустя 60 мин с момента развития острой ишемии миокарда (р<0.001, рис. 8) и оставалось низким спустя 72 часа (р<0.001, рис.8). Одновременно имело место снижение содержания восстановленного глутатиона в сыворотке крови экспериментальных животных (р<0.001, рис.9).
Выводы:
- В динамике острой ишемии миокарда отмечено одномоментное снижение содержания в миокарде и сыворотке крови восстановленного глутатиона на фоне возрастания уровня МДА. Мониторинг указанных показателей (восстановленного глутатиона и МДА) в сыворотке крови может быть использован вместе с другими биохимическими маркерами в качестве объективных критериев оценки развития деструктивных процессов в миокарде.
- Возникает стабильная недостаточность антиоксидантной системы миокарда в динамике острой ишемии миокарда, о чем свидетельствует снижение активности СОД, коррелирующее с подавлением активности каталазы гомогенатов миокарда.
- Активность ферментного звена антиоксидантной системы крови претерпевает фазные изменения: на ранней стадии ишемии возникает активация СОД и каталазы, сменяющаяся подавлением активности этих ферментов на поздних стадиях патологии.
- Возрастание супероксиддисмутазой активности сыворотки крови на ранних стадиях ишемии происходит, по-видимому, за счет усиления продукции острофазного белка - церулоплазмина и экстрацеллюлярной высокомолекулярной формы СОД. В свою очередь активация СОД сыворотки крови препятствует развитию цитопатогенных эффектов активных форм кислорода, в частности, дестабилизации мембран эндотелиоцитов и клеток крови, развитию эндотелиальной дисфункции, расстройству коагуляционного потенциала крови. Однако этот механизм компенсации истощается спустя 72 часа с момента развития острой ишемии.
- Несмотря на различие этиологических факторов и пусковых механизмов развития ишемии миокарда эфферентным звеном деструкции миокардиоцитов при указанной патологии является активация процессов липопероксидации. Последнее предопределяет целесообразность использования в комплексной терапии ишемии миокарда антигипоксантов и антиоксидантов, таких как гутимин - атмизолового ряда или олифен из класса редокс-полимеров, или цитофлавин, сочетающего в себе свойства антиоксиданта и антигипоксанта и достаточно широко апробируемого в клинической практике.
СПИСОК ЛИТЕРАТУРЫ
- Дубинина Е.Е., Сальникова Л.А., Ефимова Л.Д. Лабораторное дело, №10, 1983. - с. 30-33.
- Зайчик А.Ш., Гурилов Л.П. Основы общей патологии. Часть 2. / А.Ш. Зайчик, Л.П. Гурилов. - Основы патохимии. - СПб.: ЭЛБИ, 2000. - 687с. - с.363-364.
- Королюк М.А. и др. Лабораторное, 1988, №1. - с.16.
- Путилина Ф.Е. Методы биохимических исследований - ЛГУ, Ленинград, 1982. - с.183-187.
- Патологическая физиология и биохимия: Учебное пособие для ВУЗов / - М.: Издательство «Экзамен». 2005. - 480с. - с.140-151.
- Стальная И.Д., Гаришвили Т.Г. Современные методы в биохимии. - М.: Москва, 1977. - с.66-68.
- Типовые патологические процессы / Н.П. Чеснокова: Учебное пособие / - Издательство Саратовского медицинского университета. 2004. -с. 132-136.
- Ennor A. and H.Rosenberg. Biochem J. 51, 1952. - 606- 610.
- Selye H., Bayusz E., Crasso, and Mendell, Angiologia, 11, 1960. - 398-407.
Библиографическая ссылка
Бизенкова М.Н., Чеснокова Н.П., Романцов М.Г. О РОЛИ АКТИВАЦИИ ПРОЦЕССОВ ЛИПОПЕРОКСИДАЦИИ В МЕХАНИЗМАХ ИШЕМИЧЕСКОГО ПОВРЕЖДЕНИЯ МИОКАРДА // Современные наукоемкие технологии. 2006. № 2. С. 26-31;URL: https://top-technologies.ru/en/article/view?id=22384 (дата обращения: 07.06.2026).



