Молекулярный дизайн – это конструирование новых химических соединений с заданными свойствами, с использованием компьютерных методов моделирования. При проведении моделирования используют различные методы и подходы, одним из которых является использование множественного линейного регрессионного анализа. Математическое моделирование с использованием регрессионных моделей представляет собой построение зависимостей прогнозируемого параметра от структуры.
Молекулярный дизайн биологически активных соединений с использованием математических моделей позволяет произвести скрининг (поиск) на определенный вид биологической активности, например противовоспалительную, анальгетическую и противомикробную. Современные методы проведения скрининга основаны на использовании моделей поиска и разработанных на их основе компьютерных программ. Проведением скрининга изучают спектр биологической активности анализируемого ряда соединений и проводят отбор потенциально активных, до проведения их синтеза и биологических испытаний.
Производные антраниловой кислоты или 2-аминобензойной кислоты проявляют различные виды биологической активности, например противовоспалительную [1, 2], анальгетическую [3] и противомикробную [4–6].
Цель исследования: математическое моделирование с использованием регрессионных моделей в молекулярном дизайне соединений с противовоспалительной (ПВА), анальгетической (АА) и противомикробной активностью (ПМА) в ряду производных антраниловой кислоты.
Материалы и методы исследования
Оптимизацию структуры и расчёт квантово-химических дескрипторов исследуемых производных антраниловой кислоты, проводили с использованием программы Gaussian 03 полуэмпирическим методом РМ3, с полной оптимизации геометрии молекул. Моделирование лиганд-рецепторных взаимодействий осуществляли программой AutoDock 4.0 в составе программного комплекса MGL Tools 1.5.6, с использованием Ламарковского генетического алгоритма, который позволяет воспроизводить строение комплексов более точно. Для составления прогнозного комплекса на основе регрессионных моделей использовали Microsoft Excel 2007.
Результаты исследования и их обсуждение
Для математического моделирования при проведении молекулярного дизайна соединений с противовоспалительной, анальгетической и противомикробной активностями, предложен подход, основанный на использовании ранее составленных регрессионных моделей. С целью увеличения производительности проводимого моделирования при его практической реализации, составлен прогнозный комплекс на основе таблиц с использованием средств Microsoft Excel 2007.
В результате получили прогнозный комплекс, состоящий из четырех модулей: модуль 1 «Физико-химические свойства (константы липофильности (logP), константы ионизации (константы кислотности (рКа) и основности (pKb))»; модуль 2 «противовоспалительная активность (ПВА)»; модуль 3 «анальгетическая активность (АА)»; модуль 4 «противомикробная активность (ПМА)».
Каждый из полученных модулей разделен на модели для соответствующих рядов производных антраниловой кислоты. Валидация использованных уравнений множественной регрессии для составления моделей, приведена по следующим критериям: коэффициент корреляции (R), критерий Фишера (F), критерий оценки методом перекрестного контроля исключением по одному (Q2LOO) и среднеквадратичная ошибка (S).
Полученный прогнозный комплекс использован для проведения высокопроизводительного скрининга 203 соединений производных 5-бром(5-йод), 3,5-дихлор(3,5-дибром) антраниловой кислоты на ПВА, АА и ПМА. Результаты моделирования методом молекулярного дизайна, с использованием прогнозного комплекса, показаны на выборке, состоящей из десяти соединений, обладающих по результатам проведенного скрининга, выраженными ПВА и АА.
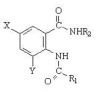
X = Br, Y = H, R1 = C6H5, R2 = C6H4(4-CH3) (1); X = I, Y = H, R1 = C6H5, R2 = C6H4(4-CH3) (2); X = Br, Y = Br, R1 = C6H5, R2 = C6H4(4-CH3) (3); X = Cl, Y = Cl, R1 = C6H4(4-CH3), R2 = C6H4(4-CH3) (4); X = Cl, Y = Cl, R1 = C6H5, R2 = C6H4(4-CH3) (5); X = Br, Y = H, R1 = 2-фурил, R2 = C6H4(4-CH3) (6); X = Cl, Y = Cl, R1 = C6H4(4-CH3), R2 = CH2CH2CH2CH3 (7); X = Cl, Y = Cl, R1 = C6H5, R2 = CH2C6H5 (8); X = Br, Y = Br, R1 = C6H5, R2 = CH2C6H5 (9); X = Cl, Y = Cl, R1 = C6H4(4-CH3), R2 = CH2C6H5 (10).
Модуль 1 «Физико-химические свойства (константы липофильности (logP), константы ионизации (константы кислотности (рКа) и основности (pKb))».
Для прогнозирования физико-химических свойств провели расчёт квантово-химических дескрипторов: суммарные значения напряженности электрического поля Σ(Е), потенциала Σ(φ) и абсолютной величины заряда Σ(|q|) на атомах кислорода, азота, углерода и водорода Σ(Н). Квантово-химические параметры рассчитаны полуэмпирическим методом РМ3 с полной оптимизацией геометрии молекул с использованием программы Gaussian 03.
Расчёт констант липофильности (logP) в модуле 1 представлен по двум моделям:
Модель 1. Производные N-арилзамещенных антраниловых кислот [7]. Модель описывает зависимость logP от дескрипторов ΣО(φ), ΣO(|q|), ΣH(φ) (R = 0,709, F = 4,06, N = 16).
Модель 2. Производные N-алкилзамещенных антраниловых кислот. Модель описывает зависимость logP от дескрипторов ΣО(Е), ΣN(Е), ΣC(φ), ΣО(φ) (R = 0,896, F = 17,31, N = 22).
Для исследуемого ряда химических соединений содержащего при атоме азота NH-ацильной группы заместители ароматической природы: фенил, 4-метилфенил, 2-фурил – использовали модель 1. Результаты прогноза logP приведены в таблице.
Модель расчёта констант ионизации (констант кислотности (рКа) и основности (pKb)) сплошная, не разделяет производные антраниловой кислоты по представителям в ряды: модель описывает зависимость рКа от дескрипторов ΣС(E), ΣN(E), ΣC(φ) (R = 0,817, F = 13,38, Q2LOO = 0,52, N = 24) и рКb от ΣС(E), ΣN(E), ΣC(φ), ΣN(φ) (R = 0,844; F = 11,78, Q2LOO = 0,55, N = 24) [8]. Результаты расчёта рКа и pKb представлены в таблице.
Модуль 2 «противовоспалительная активность (ПВА)». Основан на использовании скоринговых функций, полученных в результате молекулярного докинга производных антраниловой кислоты c ферментами циклооксигеназа (ЦОГ) 1 и 2, в качестве мишеней использовали кристаллографические копии ферментов, полученные рентгеноструктурным анализом и представленные в виде pdb-файлов, взятых из базы данных Brookhaven Protein Data Bank: ЦОГ 1 (PDB ID code: 3N8X [9]) и ЦОГ 2: (PDB ID code: 1PXX [10]). При проведении скрининга были использованы скоринговые функции: энергия связывания Be (BeЦОГ1 и BeЦОГ2), межмолекулярная энергия Ime (ImeЦОГ1 и ImeЦОГ2), константа ингибирования Ki (KiЦОГ1 и KiЦОГ2), и рассчитанные значения физико-химических свойств (logP, pKa, pKb).
Модуль 2 предназначен для количественного прогнозирования величины ПВА в процентах ( %, процент торможения карагенинового отёка) четырёх рядов производных антраниловой кислоты с использованием четырех моделей:
Модель 1. N-Замещенные антраниловые кислоты (R = 0,843, F = 23,49, S = 6,97, Q2LOO = 0,61, N = 22);
Модель 2. Замещенные амиды и гидразиды N-ароилантраниловых кислот (R = 0,902, F = 26,32, S = 8,14, Q2LOO = 0,73, N = 22) [11];
Модель 3. Гидразиды и амиды N-ацилантраниловых кислот (R = 0,859, F = 29,61, S = 9,84, Q2LOO = 0,61, N = 24);
Модель 4. Ариламиды N-ацил-N-алкенилантраниловых кислот (R = 0,920, F = 18,01, S = 8,14, Q2LOO = 0,74, N = 18).
Исследуемые производные в своей структуре при атоме азота NH-ацильной группы содержат заместители ароматической природы (фенил, 4-метилфенил, 2-фурил) и относятся к замещенным амидам и гидразидам N-ароилантраниловых кислот. Поэтому для проведения скрининга использовали модель 2, результаты расчёта ПВА приведены в таблице.
Модуль 3 «анальгетическая активность (АА)». Модуль основан на использовании скоринговых функций, полученных в результате молекулярного докинга по ферментам ЦОГ 1 и 2: энергия связывания Be (BeЦОГ1 и BeЦОГ2), межмолекулярная энергия Ime (ImeЦОГ1 и ImeЦОГ2), константа ингибирования Ki (KiЦОГ1 и KiЦОГ2), и прогнозируемых значений logP, pKa и pKb.
Модуль 3 предназначен для количественного прогнозирования величины АА (сек), двух рядов производных антраниловой кислоты, в виде моделей 1 и 2:
Модель 1. N-замещенные антраниловые кислоты (R = 0,899, F = 8,46, S = 2,27, Q2LOO = 0,51, N = 10);
Модель 2. Амиды и гидразиды N-замещенные 3,5-дибром(Н)антраниловой кислоты (R = 0,800, F = 11,85, S = 4,68, Q2LOO = 0,53, N = 24).
При прогнозировании АА исследуемых 10 соединений использовали модель 2, предназначенную для прогнозирования АА амидов N-замещенных. Результаты прогноза АА приведены в таблице.
Модуль 4 «противомикробная активность (ПМА)». Модуль основан на использовании результатов молекулярного докинга по ферменту пептид деформилаза (гидролаза) E. сoli и S. аureus. При проведении докинга в качестве мишеней использовали кристаллографические копии ферментов, полученные рентгеноструктурным анализом и представленные в виде pdb-файлов, взятых из базы данных Brookhaven Protein Data Bank: гидролаза E. сoli (PDB ID code: 1LRU [12]) и гидролаза S. аureus (PDB ID code: 1Q1Y [13]). При проведении скрининга были использованы скоринговые функции: энергия связывания Be (BeE. сoli и BeS. аureus), межмолекулярная энергия Ime (ImeE. сoli и ImeS. аureus), константа ингибирования Ki (KiE. сoli и KiS. аureus), и прогнозируемые значения физико-химических свойств (logP, pKa и pKb).
Результаты скрининга 10 соединений на ПВА, АА, ПМА(E. сoli) и ПМА(S. аureus) и физико-химические свойства (logP, pKa, pKb)
|
№ |
logP |
pKa |
pKb |
ПВА, % |
АА, сек |
ПМА(E. сoli) (мкг/мл) |
ПМА(S. аureus) (мкг/мл) |
|
1 |
2,74 |
7,05 |
13,18 |
38,85 |
20 |
1783 |
1481 |
|
2 |
2,74 |
7,05 |
13,18 |
51,04 |
19 |
1186 |
1630 |
|
3 |
2,72 |
6,93 |
13,10 |
44,08 |
13 |
635 |
2241 |
|
4 |
2,64 |
7,47 |
13,05 |
45,16 |
19 |
380 |
616 |
|
5 |
2,72 |
6,93 |
13,10 |
42,33 |
26 |
559 |
833 |
|
6 |
2,99 |
7,02 |
13,42 |
50,45 |
16 |
1189 |
1779 |
|
7 |
2,68 |
8,79 |
12,30 |
56,30 |
20 |
920 |
283 |
|
8 |
2,75 |
7,14 |
12,96 |
48,90 |
20 |
862 |
1474 |
|
9 |
2,75 |
7,14 |
12,96 |
45,00 |
15 |
663 |
1525 |
|
10 |
2,67 |
7,69 |
12,91 |
43,00 |
17 |
1168 |
1058 |
Полученный модуль 4 предназначен для количественного прогнозирования величины ПМА по E. сoli (ПМА(E. сoli)) и S. аureus (ПМА(S. аureus)) (мкг/мл), трёх рядов производных антраниловой кислоты в виде трёх моделей:
Модель 1. N-Ацилзамещенные антраниловые кислоты: скрининг на ПМА(E. сoli) (R = 0,915, F = 19,43, S = 0,30, Q2LOO = 0,72, N = 20) и ПМА(S. аureus) (R = 0,944, F = 31,03, S = 0,25, Q2LOO = 0,81, N = 20).
Модель 2. Замещенные амиды и гидразиды N-ароилантраниловых кислот: скрининг на ПМА(E. сoli) (R = 0,944, F = 31,20, S = 0,15, Q2LOO = 0,71, N = 20) и ПМА(S. аureus) (R = 0,907, F = 17,46, S = 0,21, Q2LOO = 0,68, N = 20).
Модель 3. Гидразиды и амиды N-ацилантраниловых кислот: скрининг на ПМА(E. сoli) (R = 0,901, F = 16,25, S = 0,43, Q2LOO = 0,68, N = 20) и ПМА(S. аureus) (R = 0,883, F = 18,94, S = 0,42, Q2LOO = 0,69, N = 20).
При проведении скрининга ПМА исследуемых 10 соединений использовали модель 2, предназначенную для прогнозирования ПМА амидов N-ароилзамещенных антраниловой кислоты. Результаты прогноза ПМА приведены в таблице.
Таким образом, проведено моделирование исследуемого ряда на три вида биологической активности (ПВА, АА и ПМА) и выполнен расчёт физико-химических свойств, результат представлен в таблице.
Рассчитаны физико-химические свойства (константы липофильности и ионизации). Максимальное значение липофильности рассчитано для соединения 6 (logP = 2,99), минимальное – у соединения 4 (2,64). Наибольшее значение константы кислотности спрогнозировано для соединений 3 и 5 (рКа = 6,93). Прогнозируемые значения констант основности лежат в интервале 12,30–13,42.
В результате проведенного скрининга обнаружено, что все проанализированные соединения будут обладать выраженной ПВА (свыше 30 %), по АА (свыше 19 с), только соединения под номерами 1, 2, 4, 5, 7 и 8. По ПМА прогнозный уровень слабый (от 250 до 1000 мкг/мл) или неактивный (свыше 1000 мкг/мл), перспективных, с ПМА менее 2 мкг/мл не обнаружено. По результатам экспериментального исследования на прогнозируемые активности, получен патент на структуру 1, как соединение обладающее выраженной ПВА [14].
Заключение
Проведенные исследования показали возможность молекулярного дизайна путем изменения структуры, с использованием полученной математической модели, с целью получения соединений с заданными свойствами и уровнем биологической активности.
Таким образом, можно сделать вывод, что составленный прогнозный комплекс, полученный в результате математического моделирования, на основе регрессионных уравнений и Microsoft Excel 2007, может быть использован в молекулярном дизайне соединений с противовоспалительной, анальгетической и противомикробной активностью производных антраниловой кислоты.
Библиографическая ссылка
Андрюков К.В., Коркодинова Л.М. МАТЕМАТИЧЕСКОЕ МОДЕЛИРОВАНИЕ С ИСПОЛЬЗОВАНИЕМ РЕГРЕССИОННЫХ МОДЕЛЕЙ В МОЛЕКУЛЯРНОМ ДИЗАЙНЕ СОЕДИНЕНИЙ С ПРОТИВОВОСПАЛИТЕЛЬНОЙ, АНАЛЬГЕТИЧЕСКОЙ И ПРОТИВОМИКРОБНОЙ АКТИВНОСТЬЮ ПРОИЗВОДНЫХ АНТРАНИЛОВОЙ КИСЛОТЫ // Современные наукоемкие технологии. 2019. № 9. С. 31-35;URL: https://top-technologies.ru/ru/article/view?id=37661 (дата обращения: 13.05.2026).



