Галогенсодержащие производные адамантана (ГПА) представляют интерес как ценные полупродукты для получения различных биологически активных производных адамантана, мономеров для синтеза полимерных материалов. Использование 1,3-дегидроадамантана 1 (ДГА) в качестве адамантилирующего агента позволяет исключить некоторые недостатки существующих методов синтеза таких соединений, а также значительно расширить их ассортимент. Кроме того открываются возможности получения труднодоступных ГПА в одну стадию, а также осуществить реакции, нетипичные для некоторых классов соединений [1-5].
Ранее, в реакциях ДГА с галогенкарбоновыми кислотами Hal-СН2-СООН, установлена зависимость селективности реакций от природы галогена [4]. Так, селективность реакции ДГА по связи С-Hal увеличивалась в ряду J > Br > Cl > F >. В этой связи, интересным было установить, сохраняются ли эти закономерности в реакциях с другими классами галогенсодержащих соединений, например с хлораренами: бензилхлоридом и фенилхлороформом.
Реакцию 1,3-ДГА с хлористым бензилом проводили в атмосфере сухого, очищенного от кислорода азота, в отсутствии растворителя, при температуре 110 0С, в течение 2 часов, при 2-х кратном мольном избытке хлористого бензила. Реакция 1,3-ДГА с бензилхлоридом привела к получению смеси продуктов присоединения по связям С- H и C-Cl в соотношении 2а : 2b – 8 : 1 с суммарным выходом 75 %.
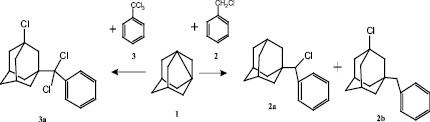
Кроме того, в продуктах реакции обнаружен 1,1’-диадамантил (~ 2 %), 1-хлорадамантан (~ 5 %), а также (3-хлорадамант-1-ил)фенилхлорметан (~ 8 %) и бензиладамантан (~ 4 %). Таким образом, и в случае бензилхлорида проходят конкурентные реакции ДГА как по связи С-Н так и по связи С-Cl. При этом преобладают превращения по связи С-Н. Образование широкого спектра продуктов реакции говорит о вероятном радикальном механизме реакций с участием 1,3-бирадикала адамантана, образующегося при термолизе пропеллановой связи ДГА.
Реакцию 1,3-ДГА с фенилхлороформом проводили в среде тетрагидрофурана, в атмосфере сухого, очищенного от кислорода азота, при температуре 70 0С, в течение 2 часов, при 3-х кратном мольном избытке фенилхлороформа. Взаимодействие 1,3-ДГА с фенилхлороформом 3, протекало только по связи С-Cl с образованием 1,3-дизамещенного адамантана – (3-хлор-адамант-1-ил)дихлорфенилметана 3а в одну стадию с выходом 91 %. Аналогично ДГА реагировал с этиловым эфиром трихлоруксусной кислоты [4, 5].
Состав и строение полученных продуктов подтверждены методами тонкослойной хроматографии, хромато–масс–спектрометрии, элементным анализом. 1Н ЯМР-спектроскопией. Характерной особенностью масс-спектров 2b и 3а является присутствие пика с m/z 133, соответствующего 1,3-дизамещенному адамантану. Самым интенсивным является пик иона с m/z 169, который соответствует хлорадамантильному катиону, а в спектре 2а – пик с m/z 135-адамантильному катиону. Также на спектре 3а присутствуют пики ионов, соответствующие последовательному отщеплению атомов хлора: m/z 293, 257 и 223.
Полученные соединения могут использоваться как полупродукты в синтезе широкого спектра различных, в том числе биологически активных веществ.
Библиографическая ссылка
Лагутин П.А., Бутов Г.М., Дьяконов С.В. РЕАКЦИИ 1,3-ДЕГИДРОАДАМАНТАНА С ХЛОРСОДЕРЖАЩИМИ АРЕНАМИ // Современные наукоемкие технологии. 2013. № 9. С. 81-82;URL: https://top-technologies.ru/ru/article/view?id=33232 (дата обращения: 07.06.2026).



