Цель: определение возможности замены мерной пипетки на мерный цилиндр в студенческом лабораторном практикуме по химии для упрощения лабораторной работы по определению концентрации щелочи титрованием.
В работе использовался метод кислотно-основного титрования, основанный на применении реакции нейтрализации
2NaOH + H2SO4 = Na2SO4 + 2H2O.
К раствору определяемого вещества – гидроксида натрия – постепенно прибавляли раствор серной кислоты известной концентрации до тех пор, пока его количество не становилось эквивалентным количеству гидроксида натрия, вступившего в реакцию, т.е. до нейтрализации щёлочи. Момент нейтрализации устанавливали по изменению окраски индикатора, прибавляемого в титруемый раствор.
Молярную концентрацию эквивалента щелочи определяли из закона эквивалентов по уравнению
![]() ,
,
где Сн(NaOH) и Сн(H2SO4) – молярные концентрации эквивалента NaОН и H2SO4 в реагирующих растворах, моль/л; V(NaOH) и V(H2SO4) – объёмы реагирующих растворов щёлочи и кислоты, мл.
Для титрования использовалась установка, изображенная на рисунке.
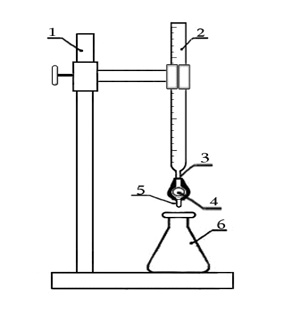
Установка для титрований: 1 – штатив; 2 – бюретка; 3 – резиновая трубка; 4 – олива; 5 – носик бюретки; 6 – колба
Провели 10 параллельных опытов. Результаты титрований занесены в табл. 1.
Таблица 1
Результаты титрования раствора гидроксида натрия
|
№ |
Объём пробы раствора щёлочи V(NaOH), мл |
Объём раствора кислоты V(H2SO4), мл |
Молярная концентрация эквивалента щёлочи Сн (NaOH), моль/л |
Среднее значение молярной концентрации эквивалента NaOH в анализируемом растворе, моль/л |
|
1 |
25 |
19,78 |
0,07912 |
0,79256 |
|
2 |
25 |
19,88 |
0,07952 |
|
|
3 |
25 |
19,77 |
0,07908 |
|
|
4 |
25 |
19,81 |
0,07924 |
|
|
5 |
25 |
19,83 |
0,07932 |
|
|
6 |
25 |
19,88 |
0,07952 |
|
|
7 |
25 |
19,79 |
0,07916 |
|
|
8 |
25 |
19,80 |
0,0792 |
|
|
9 |
25 |
19,76 |
0,07904 |
|
|
10 |
25 |
19,84 |
0,07936 |
Провели статистическую обработку результатов (табл. 2), определив значение выборочной дисперсии ![]() , среднеквадратичную ошибку (стандартное отклонение)
, среднеквадратичную ошибку (стандартное отклонение) ![]() и доверительный интервал в виде
и доверительный интервал в виде
![]() .
.
Таблица 2
Результаты статистической обработки экспериментальных данных титрования раствора гидроксида натрия. Доверительная вероятность a=0,95.
|
n |
|
|
Sx |
|
|
10 |
0,079256 |
0,0000025 |
0,00158 |
0,002 |
Доверительный интервал является достаточно узким, что показывают результаты статистической обработки. Доверительный интервал определен как
Сн(NaOH) = (0,079±0,002) моль/л; n=10; α=0,95.
В результате проведенных исследований можно сделать вывод, что замена мерной пипетки на более простой в работе мерный цилиндр является возможной.
Библиографическая ссылка
Правилова С.Д., Чаплинский Е.Ф., Иванова Т.А. ОПРЕДЕЛЕНИЕ КОНЦЕНТРАЦИИ ЩЕЛОЧИ В ЛАБОРАТОРНОМ ПРАКТИКУМЕ ПО ХИМИИ // Современные наукоемкие технологии. 2013. № 9. С. 62-63;URL: https://top-technologies.ru/ru/article/view?id=33203 (дата обращения: 17.05.2026).



