В золоторудных месторождений часто встречаются пирротин и пирит – природные минералы сульфидов железа состава Fe1-nS и FeS2 соответственно. Природные сульфиды железа – пирротин и пирит, часто образуются при гидротермальных процессах и подвергается активному преобразованию в экзогенных условиях [10]. Отмечается в литературе часто встречаемые залежи пирита на дне водоемов в виде донных отложений. Генезис и история формирования этих минералов имеет немаловажное значение для понимания процессов формирования золоторудных месторождений и положений золотоносных пластов в породе.
Одной из отличительных особенностей является то, что в структуре пирита атомы серы находятся в связанном в пары состоянии, образуя двухвалентную «гантель» (S2)-2, тогда как в структуре пирротина сера представлена одиночными двухвалентными ионами [10]. Поэтому анионная вакансия в структуре пирита означает отсутствие не одного иона серы, а гантели из двух связанных ионов серы. Появление катионных или анионных вакансий деформируют кристаллическую структуру иногда до такой степени, что его элементарная ячейка уже может не быть кубической. При уточнение сингонии кристаллической структуры такого пирита обнаруживается триклинная симметрия элементарной ячейки [3].
Спектры ЯГР пирита с идеальной структурой представляют собой две хорошо разрешенные линии одинаковой интенсивности – дублет, но на практике ширина и интенсивность этих линий в спектрах ЯГР природного пирита не только может изменяться, но в ряде случаев в спектре пирита появляется третья линия [9]. Все это, в итоге, свидетельствует о деформации кристаллической структуры, а, следовательно, наличие в структуре пирита катионных и анионных вакантных позиций. Влияние плотности вакантных позиций на структуру и свойства пирита практически не исследованы, хотя вакантные позиции в структуре пирротина достаточно детально описаны, например, в работах Онуфриенка [2].
До настоящего времени нет ясности в механизме формирования пирита, который не может существовать выше 398 °С [2, 3, 10]. Существует точка зрения, что пирит – это минерал, способный сформироваться при определенных условиях непосредственно из железы и серы. В ряде других работ отмечается, что низкотемпературный синтез приводит в итоге к образованию анизотропного пирита [3], а это означает, что при формировании пирита неизбежно в структуре возникают катионные или анионные вакантные позиции. Их влияние на фазовый состав и физико-химические свойства практически не исследовано. Отмечается, что пирит более симметричной структуры формируется при более высоких температурах [2, 3, 10], однако и в этом случае не исключена возможность возникновение вакантных позиций в структуре пирита. Анализ многолетнего авторского экспериментального материала ставят под сомнение факт образования пирита в результате непосредственного соединения серы и железа, минуя промежуточные стадии формирования определенной цепочки минеральных преобразований. Этот факт подтвержден рядом экспериментальных работ [5,8], в которых детально описан процесс трансформации различного рода минералов, в результате которых образуется пирит. Действительно, при формировании структуры пирита ионы серы должны первоначально сформироваться в гантель, а для этого необходимы какие-то процессы, вынуждающие ионы серы образовывать такую связь между собой. Например, пирит может образовываться из обогащенного серой пирротина с высокой плотностью катионных вакансий [2].
Цель исследования: на примере синтетических метастабильных сульфидов железа различного химического и фазового состава изучить процессы трансформации пирротина в пирит. Показать особенности трансформации сульфидов железа в фазовое состояние, когда сера в структуре связанна в гантели S2. Определить равновесные фазовые соотношения в минеральной смеси, сформировавшейся из пирита и пирротина. На основе результатов EPMA минерального состава рассчитать плотности катионных и анионных вакансий в структуре природного пирита и сопоставить результаты с содержанием золота в руде.
Материал и методы исследования
Образцы синтезировались в результате сухого синтеза в вакууме при температуре 1000 °C в течение двух суток с последующей закалкой в жидкий азот или медленного охлаждения вместе с муфельной печью в течении 20 часов до комнатной (20 °С) температуры. Соотношение S/Fe в шихте изменялось от 1 до 2,5. Пирротины получались также в результате термического разложения природного монокристаллического пирита при температурах от 350 до 1200 °С. Измельченный пирит помещался в один конец длинной (~ 2 м) кварцевой трубки с откаченным воздухом, который и помещался в середину цилиндрической печи длиной 0,75 м. Второй конец трубки находился при комнатной температуре. При прокаливании пирита пары серы конденсировались на стенках холодной части кварцевой трубки. Таким образом, в этих опытах исследовались экспериментально два процесса – синтез пирита и его разложение. Исследовался также природный пирит из участка Михайловский месторождения «Панимба» в Енисейском кряже.
Полученные образцы анализировались методами рентгеноструктурного анализа и ядерного магнитного резонанса. РФА анализ синтезированных образцов производился на дифрактометре XRD-7000 $ фирмы Shimadzu с использованием рентгеновского излучения Сu(Кα). Фазовый состав образцов определялся по методу, предложенному Дубининым [4]. Спектры ядерного гамма-резонанса (ЯГР) снимали на спектрометре с равноускоренно движущимся источником Сг (57Со). Химический состав природного пирита определен на рентгеноспектральном микроанализаторе «Camebax-Micro» (Франция, 1981 г.) в лаборатории микрозондового анализа института геологии и минералогии СО РАН, г. Новосибирск; содержание золота в пиритсодержащих интервалах пород определены в пробирной лаборатории Олимпиадинского ГОКа, официальный сайт «Полюс Золото».
Результаты исследования и их обсуждение
В результате синтеза получались в основном многофазные образцы, в состав которых входили сульфиды железа пирротин, троилит, смайтит, пирит и , после многолетней выдержки (~30 лет), формировался сомольнокит, парабутлерит, розенит гетит. Гомогенные образцы пирита в результате синтеза и последующей выдержки образцов не удалось получить даже при соотношении S/Fe ≈ 2,5 в шихте.
На рис.1 представлены рентгеновские дифрактограммы синтезированных образцов с различным соотношением пирита, пирротина и кристаллической серы.
Как следует из анализа экспериментального материала, представленного на рис. 1 в виде только двух наиболее характерных рентгеновских дифрактограмм, с увеличением температуры синтеза и содержания серы в шихте процентное содержание пирита возрастает, а пирротина уменьшается. Отметим, что первоначально синтезируется пирротин даже если в шихте достаточно серы, а только потом возникает пирит. Образцы, не содержащие пирротин, а содержащие пирит даже в равновесии с другими синтетическими минералами не были получены при любом соотношение железа и серы. Содержание пирита более 76 % в образцах получить не удалось, а пирротин всегда присутствовал во всех образцах, содержащих пирит. Поскольку пирит в принципе не может существовать при температурах, выше 500 °С, следовательно, он возникает в процессе охлаждения образцов из пирротина.
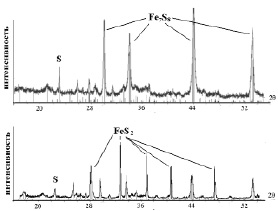
Рис. 1. Рентгеновские дифрактограммы синтетических сульфидов с различным содержанием пирита, пирротина и серы. Процентное содержание в образцах пирита: а – 11.18 %, б – 64.1 %; пирротина: а – 58.25 %, б – 27.2 %; кристаллической серы: а – 20.36 %, б – 7,1 %
Как следует из анализа экспериментального материала, представленного на рис. 1 в виде только двух наиболее характерных рентгеновских дифрактограмм, с увеличением температуры синтеза и содержания серы в шихте процентное содержание пирита возрастает, а пирротина уменьшается. Отметим, что первоначально синтезируется пирротин даже если в шихте достаточно серы, а только потом возникает пирит. Образцы, не содержащие пирротин, а содержащие пирит даже в равновесии с другими синтетическими минералами не были получены при любом соотношение железа и серы. Содержание пирита более 76 % в образцах получить не удалось, а пирротин всегда присутствовал во всех образцах, содержащих пирит. Поскольку пирит в принципе не может существовать при температурах, выше 500 °С, следовательно, он возникает в процессе охлаждения образцов из пирротина.
Определенный интерес представляет анализ образцов, содержание пирита в которых превышает 76 %, т.е. интервал 76-100 %. Образцы с таким процентным соотношением пирита были получены только в результате термического разложения природного пирита в вакууме. Если поместить в ампулу природный монокристаллический пирит, то после ее прокаливании в течении различного интервала времени в муфельной печи при t = 1000 °С получены образцы в интервале заданного фазового состава. Опыты по термическому разложению пирита показали многофазность полученных образцов, состоящих из пирит, пирротина различного состава и кристаллической серы. Отметим также, что на рентгеновских снимках, полученных с различной скоростью съемки, чистое железо (α-Fe) в образцах, полученных в результате термического разложения пирита, не фиксировалось. Если бы пирит мог формироваться непосредственно соединением серы с железом, минуя стадию пирротина, то и при разложении пирита существовала бы отличная от нуля вероятность обратного процесса – восстановления чистого железа и серы. Однако этого в экспериментах ни разу не наблюдалось.
На рис. 2 представлен спектр ЯГР образца, состоящего из ферримагнитного моноклинного пирротина и парамагнитного пирита.
Магнитное упорядочение в пирротине доказывает три секступлета в спектре, обусловленные различными магнитными полями на ядрах ионов железа в различных позициях. Эти позиции соответствуют положениям ионов железа без вакансий, с двумя вакансиями и четырьмя вакансиями во второй координационной сфере [2]. Расчетное значения полей –304 кЭ, 253 кЭ и 227 кЭ соответственно. Отметим, что значения напряженности магнитных полей на ядрах, а также значения химического сдвига, не подтверждают наличие в кристаллической структуре пирротина ионов трехвалентного железа. Центральный парамагнитный дублет в спектре ЯГР обусловлен наличием в образце парамагнитного пирита, в котором ионы железа также находятся в двухвалентном состоянии.
В таблице представлены результаты микрозондового анализа природного пирита рудника «Михайловский» золоторудного месторождения «Панимба».
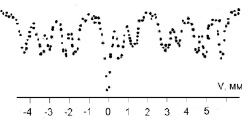
Рис. 2. Спектр ЯГР образца, состоящего из ферримагнитного моноклинного пирротина и парамагнитного пирита
Таблица
Результаты микрозондового анализа (EPMA) и результаты расчетов плотности примесных атомов в пирите
|
S/Fe (эксп.) |
S/Fe (расч) |
Плотность вакансий |
Fe+2 α |
(S2)-2 β |
Fe+2 мас. % |
(S2)-2 мас. % |
Au, г/т (в руде) |
|
2,05 |
2,051 |
0,01703 |
0,9829 |
1,0085 |
45,79 |
53,95 |
0,3 |
|
1,93 |
1,930 |
–0,02370 |
1,0237 |
0,9881 |
47,57 |
52,73 |
0,3 |
|
2,01 |
2,012 |
0,00412 |
0,9958 |
1,0020 |
46,24 |
53,43 |
0,3 |
|
2,01 |
2,008 |
0,00283 |
0,9971 |
1,0014 |
46,13 |
53,20 |
0,3 |
|
1,99 |
1,987 |
–0,00432 |
1,0043 |
0,9978 |
46,19 |
52,70 |
0,3 |
|
2,00 |
1,997 |
–0,00099 |
1,0009 |
0,9995 |
46,44 |
53,25 |
0,3 |
|
2,00 |
1,995 |
–0,00157 |
1,0015 |
0,9992 |
46,14 |
52,86 |
1 |
|
1,98 |
1,981 |
–0,00608 |
1,0060 |
0,9969 |
46,47 |
52,88 |
1 |
|
2,07 |
2,065 |
0,02142 |
0,9785 |
1,0107 |
45,52 |
53,99 |
1 |
|
1,97 |
1,969 |
–0,01012 |
1,0101 |
0,9949 |
46,53 |
52,63 |
1 |
|
1,99 |
1,986 |
–0,00446 |
1,0044 |
0,9977 |
46,20 |
52,70 |
1 |
|
2,02 |
2,019 |
0,00637 |
0,9936 |
1,0031 |
45,98 |
53,31 |
1 |
|
1,98 |
1,979 |
–0,00699 |
1,0069 |
0,9965 |
46,63 |
52,99 |
1 |
|
1,95 |
1,951 |
–0,01627 |
1,0162 |
0,9918 |
47,36 |
53,08 |
0,9 |
|
1,95 |
1,953 |
–0,01579 |
1,0157 |
0,9921 |
47,30 |
53,05 |
0,9 |
|
2,01 |
2,005 |
0,00173 |
0,9982 |
1,0008 |
46,38 |
53,40 |
0,9 |
|
1,99 |
1,992 |
–0,00234 |
1,0023 |
0,9988 |
46,49 |
53,20 |
0,9 |
|
2,03 |
2,028 |
0,00954 |
0,9904 |
1,0047 |
45,83 |
53,39 |
0,9 |
|
1,99 |
1,990 |
–0,00325 |
1,0032 |
0,9983 |
46,44 |
53,07 |
0,9 |
|
2,03 |
2,029 |
0,00987 |
0,9901 |
1,0049 |
45,97 |
53,58 |
1 |
|
2,04 |
2,036 |
0,01216 |
0,9878 |
1,0060 |
45,88 |
53,66 |
1 |
|
2,01 |
2,014 |
0,00486 |
0,9951 |
1,0024 |
45,48 |
52,61 |
1 |
|
1,99 |
1,986 |
–0,00438 |
1,0043 |
0,9978 |
45,94 |
52,41 |
1 |
|
1,98 |
1,981 |
–0,00608 |
1,0060 |
0,9969 |
45,96 |
52,30 |
1 |
|
2,00 |
2,001 |
0,00035 |
0,9996 |
1,0001 |
46,92 |
53,91 |
0,1 |
|
1,98 |
1,976 |
–0,00785 |
1,0078 |
0,9960 |
47,06 |
53,41 |
0,1 |
|
1,98 |
1,982 |
–0,00579 |
1,0057 |
0,9971 |
46,45 |
52,88 |
0,1 |
|
1,98 |
1,982 |
–0,00588 |
1,0058 |
0,9970 |
47,15 |
53,67 |
0,1 |
|
1,95 |
1,947 |
–0,01794 |
1,0179 |
0,9910 |
47,21 |
52,78 |
0,1 |
|
1,95 |
1,952 |
–0,01611 |
1,0161 |
0,9919 |
47,34 |
53,07 |
0,1 |
|
1,95 |
1,954 |
–0,01524 |
1,0152 |
0,9923 |
47,35 |
53,15 |
0,1 |
|
1,97 |
1,968 |
–0,01065 |
1,0106 |
0,9946 |
47,16 |
53,30 |
0,1 |
|
1,95 |
1,951 |
–0,01642 |
1,0164 |
0,9917 |
47,13 |
52,81 |
0,1 |
|
2,04 |
2,040 |
0,01338 |
0,9866 |
1,0066 |
45,19 |
52,95 |
0,5 |
Как следует из анализа результатов микрозондового анализа природного пирита, его состав практически всегда является нестехиометрическим, поэтому состав природного пирит лучше представлять химической формулой (Fe+2)α((S2)-2)β. Таким образом, «гантель» из двух ионов серы удобнее представлять одной формульной единицей, поэтому и плотность анионных вакантных позиций – это не что иное, как плотность таких «гантелей».
Если α и β равны 1 (стехиометрический состав FeS2), то, как показывает расчет, железа в образце должно составлять 46,5472 мас. %, а серы – 53,4528 мас. %. Отличие результатов микрозондового анализа образца от этих расчетных значений железа и серы указывает на наличие катионных или анионных вакантных позиций в структуре пирита. Как следует из таблицы, даже если для образца выполняется соотношение S/Fe=2,00 в структуре пирита и в этом случае возможны вакантные позиции. Поскольку пирит исследовался из золоторудного месторождения, интерес представляет сопоставить плотность вакантных позиций с содержанием золота в руде.
На рис. 2 представлено содержание золота в руде в зависимости от плотности вакантных позиций в структуре пирита. Положительные значения Х выражают значения плотности катионных вакантных позиций, а отрицательные значения – плотности анионных вакантных позиций.
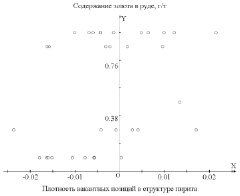
Рис. 3. Содержание золота в руде в зависимости от плотности вакантных позиций в структуре пирита
На основе анализа таблицы и рис. 3 можно отметить условное деление пирита на два химических типа минерала – обогащенного и обедненного серой. Из рис. 3 видно, что золота больше в такой породе, в которой пирит содержит в структуре вакантные анионные позиции, т.е. дефицит «гантелей» из ионов серы.
Дискуссия. Для аргументации того, что переход пирротина в пирит может быть индуцирован именно катионными вакансиями рассмотрим детально кристаллическое строение пирита и пирротина. Пирротин Fe1-n S (n – число катионных вакансий в молекуле) относится к группе соединений сульфидов железа, обладающих кристаллической структурой типа NiAs. На рис. 1 слева представлена структура NiAs. Структура NiAs характеризуется гексагональной плотной упаковкой анионной подрешетки, в октаэдрических междоузлиях которой расположены катионы, образующие простую гексагональную решетку. Эта структура обладает гексагональной голоэдрической симметрией (класс 6/mmn) и пространственной группой P6/mmc Октаэдрические междоузлия, расположенные вдоль оси «с», имеют общие грани сверху и снизу, так, что катионы располагаются в виде линейной цепочки. В базисной плоскости октаэдры имеют общее ребро [10].
Характерной особенностью пирротина является его химическая и структурная неоднородность. В его базисной элементарной ячейке кристаллической структуры содержатся два катиона двухвалентного железа и два аниона серы, причем часть катионных позиций вакантна [2, 10]. Если влияние температуры, давления, концентрации катионных вакансий на фазовые переходы нестехиометрических сульфидов железа широко исследуются [7–9], то практически нет работ по изучению влияния анионных вакансий (представляющих собой связанные в гантель ионы серы) на процессы кристаллохимических фазовых переходов.
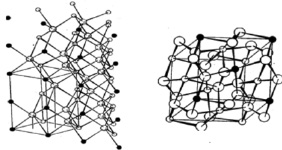
Рис. 4. Кристаллическая структура типа NiAs (а) и кристаллическая структура пирита (б)
В структуре пирита (рис. 1 справа) атомы железа образуют ГЦК – подрешетку, а атомы S располагаются парами таким образом, что центры тяжести этих пар занимают середины ребер элементарной ячейки и ее центр. Структуру пирита можно рассматривать как структуру типа NaCl, в которой атомы Na замещены атомами Fe, а атомы Cl – парами атомов S. Оси «гантелей» S2 располагаются под углом к направлению (100) вдоль четырех тройных непересекающихся осей структуры. Параметр идеальной (не искаженной) элементарной ячейки пирита a = 5,41 Å. Таким образом, пирит обладает кубической структурой, в которой, в отличие от структуры пирротина, анионы сформированы в двухвалентные гантели, состоящие из двух атомов серы [5].
Общее для пирротина и пирита является наличие ионов железа в двухвалентном состоянии. До настоящего времени ряд исследователей пытается приписать наличие в структуре пирротина ионов железа в трехвалентном состоянии, забывая, что пирротин нестехиометрического состава является полупроводником, поэтому обладает собственной проводимостью, т.е. концентрация электронов в зоне проводимости отлична от нуля. Если на каком-то узле кристаллической структуры возникает необходимость в электроне, то его не надо отрывать из d-орбитали и делать ион железа трехвалентным – для этого достаточно захватить его из зоны проводимости, понизив концентрацию в ней электронов, а, следовательно, сместив проводимость в область p-типа, т.е. дырочной. В структуре моноклинного пирротина достаточно высокая (~ 0,125) плотность катионных вакансий. Если моноклинный пирротин перенасыщен серой и находится в метастабильном состоянии, то плотность вакансий может превышать максимально-допустимую для стабильного фазового состояния. В таком случае, вакансии могут иметь частичное разупорядочение, т.е. их симметричное расположение в структуре может быть нарушено до такой степени, что в структуре возможно образование нано – областей с повышенной плотностью катионных вакансий. Можно предположить, что ионы серы в зонах с повышенной концентрацией катионных вакансий образуют между собой ковалентную связь, образуя двухвалентную гантель из двух атомов серы. В этом случае два электрона присоединяют для связи уже не один ион серы, а сразу два. Таким образом, с образованием гантелей из ионов серы понижается необходимая плотность двухвалентных ионов железа. Пока концентрация гантелей из атомов серы достаточно мала, фазовый переход пирротин – пирит не происходит. Но когда их концентрация достигает некоторого критического значения – реализуется фазовый переход пирротин – пирит. Таким образом, в данном случае можно считать, что этот фазовый переход индуцирован катионными вакансиями, пирротин является необходимым звеном в минералогической цепи формирования двухвалентных гантелей из атомов серы, необходимых для образования пирита. В противном случае, свободная сера никогда не станет организовываться и образовывать «гантелей», необходимые для формировании кубической гранецентрированной структуры пирита, «гантели» из ионов серы в которой расположены на ребрах куба.
Выводы
Экспериментально исследован переход синтетического пирротина в структуру пирита. Предложена модель формирования пирита из пирротина, основанная на анализе плотности катионных вакансий в структуре пирротина. В рамках предложенной модели показано, что пирит не образуется без промежуточной минеральной фазы, необходимой для формирования двухвалентных «гантелей» из двух ионов серы.
На примере пирита месторождения «Панимба» доказано, что пирит практически всегда не обладает стехиометрическим составом, а, следовательно, имеет катионные и анионные вакантные позиции в структуре. Разработан алгоритм расчета плотности катионных и анионных вакантных позиций в кубических структурах типа пирита. На основе результатов микрозондового анализа минерального состава (EPMA – electron-probe micro-analysis) рассчитаны плотности катионных и анионных вакансий в структуре природного пирита золоторудного месторождения «Панимба». Предложено деление минерала на два химических типа – обогащенного и обедненного серой. Установлено, что содержание золота преобладает в такой породе, в которой пирит имеет дефицит «гантелей» из ионов серы в структуре.
Библиографическая ссылка
Онуфриенок В.В. КРИСТАЛЛОХИМИЧЕСКОЕ ПРЕВРАЩЕНИЕ ПИРРОТИН-ПИРИТ, ИНДУЦИРОВАННОЕ КАТИОННЫМИ ВАКАНСИЯМИ // Современные наукоемкие технологии. 2013. № 5. С. 116-122;URL: https://top-technologies.ru/ru/article/view?id=31813 (дата обращения: 07.06.2026).



