В данной работе проводили полимеризацию акриловой кислоты (АК) на природном бентоните (месторождение Казахстана) в присутствии инициатора (ПБ) с целью получения органоминерального карбоксильного катионита.
При обработке поверхности минерала инициатором последний внедряется в структуру и сохраняет способность для инициирования процесса. При проведении полимеризации АК в присутствии обработанной инициатором поверхности образуется прочная связь полимера с поверхностью и происходит прививка.
В условиях проведенных опытов поверхность бентонита покрыта водой и не является катализатором полимеризации.
Экстракционные данные показали, что некоторая часть полимера не удаляется растворителем, что дает основание полагать, что произошла прививка ПАК на бентоните.
Образование химической связи полимера с минеральным носителем подтверждается данными ИК-спектроскопии образцов, подвергнутых экстракции от гомополимера. В спектрах этих продуктов наряду с полосами поглощения, характерными для минеральных соединений, присутствуют и полосы поглощения привитого полимера (1690-1720 см-1).
В принятых условиях полимеризации получены продукты с различным содержанием привитого (от веса продукта) к минералу полимера.
Основными факторами, оказывающими влияние на процесс полимеризации на поверхности минерального носителя, являются содержание мономера, концентрация инициатора в системе.
С возрастанием содержания акриловой кислоты количество привитого полимера увеличивается, дальнейшее же повышение его незначительно влияет на привес ПАК, поскольку в среде чистого мономера и при высоких его концентрациях протекает процесс гомополимеризации.
С увеличением содержания инициатора от 0,1-0,4 %, т.е. в пределах концентраций, обычно применяющихся в практике проведения радикальной полимеризации виниловых мономеров, количество привитого полимера возрастает.
Полимеризация АК на природном бентоните в течение 60 минут позволяет получить минерально-органический продукт, содержащий 13 % химически привитого полимера. Статическая обменная емкость катионита по 0,1н раствору КОН составляет 7,5 мг-экв/г.
В дальнейшем модифицированный бентонит использовали для сорбции ионов меди (II).
Результаты исследования кинетики процесса сорбции ионов меди (II) показали, что равновесие в распределении ионов металла между твердой фазой и раствором при комнатной температуре устанавливается за 30 мин, при этом извлечение проходит наиболее полно модифицированным бентонитом (99,5 %), чем КБ-4 (95,0 % за 60 мин) (рис.1). Высокая удельная поверхность (265 м2/г) природного минерала обусловливает быструю сорбцию катионов (60 % за 15 мин). Однако наличие химически активных групп на поверхности модифицированного бентонита определяет его высокие обменные свойства.
Извлечение ионов меди (II) из раствора исследуемым катионитом, содержащим на поверхности карбоксильные группы может осуществляться за счет образования как ионной, так и координационной, а в некоторых случаях только координационной связи, энергия которой определяет селективность ионита по отношению к компонентам раствора. Количество привитых групп, способных реагировать с ионами металла, существенно зависит от кислотности среды. Исследование влияния рН на сорбцию ионов металла органоминеральным катионитом и КБ-4 показывает (рис.2), что процесс начинается еще в кислой области, и степень извлечения возрастает от 49,6 до 99,7 % (8,45-16,80 мг/г), а для промышленного катионита в аналогичных условиях извлекается 26,0-92,0 % (7,45-15,11 мг/г) ионов меди. Степень извлечения достигает максимальных значений при рН>5, где предполагается, что высокая устойчивость комплекса, так как при низких значениях рН сорбент находится в протонированном состоянии. Однако в этом случае обычно образуются гидролизованные формы металла. В процессе сорбции использовали катионит в Н+-форме, поэтому отмечалось понижение величины рН равновесного раствора за счет перехода протонов в раствор при координации ионов меди с карбоксильными группами сорбента.
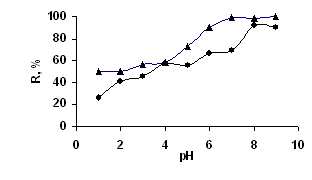
Рисунок 1. Зависимость степени извлечения ионов меди (II) сорбентами от продолжительности сорбции
▲ -органоминеральный катионит, ● - КБ-4, ■ - бентонит СCu2+=0,5 г/л, V=50 мл, mc=0,5 г
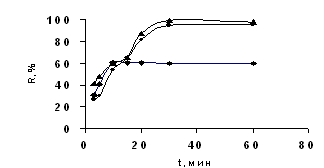
Рисунок 2. Влияние рН на степень извлечения ионов меди (II) органоминеральным катионитом ▲ -органоминеральный катионит, ● - КБ-4 t = 30 мин, СМе2+=0,25 г/л, V=10 мл, mc=0,1г
Для определения возможности извлечения ионов меди из растворов, содержащих ионы никеля и кобальта с суммарной концентрацией всех ионов 0,375 г/л исследовали влияние продолжительности процесса на степень извлечения каждого катиона. Показано, что органоминеральный катионит по сорбционной активности не уступает промышленному сорбенту. Кинетика процесса извлечения ионов цветных металлов на исследуемых сорбентах является замедленной, за 120 мин поглощение ионов меди происходит на 90 % на модифицированном бентоните и 79,5 % на КБ-4. Установлено, что модифицированный бентонит проявляет некоторую избирательность по отношению к ионам меди по сравнению с КБ-4. Представленные значения коэффициентов распределения изменяются в следующем ряду Cu2+ > Ni2+ ≈ Co2+ (табл.).
Таблица1. Коэффициенты распределения ионов тяжелых металлов (условия сорбции: 120 мин, ΣСМе=0,375 г/л, СМе=0,125 г/л, Ж/Т = 10)
|
Ионы |
D, л/г |
|
|
Органоминеральный катионит |
КБ-4 |
|
|
Cu2+ Co2+ Ni2+ |
2,20 0,60 0,51 |
1,50 1,30 0,48 |
В результате проведенных исследований установлено, что бентонит, содержащий на поверхности привитые группы полиакриловой кислоты, в сопоставимых условиях значительно лучше извлекает ионы меди (II) по сравнению с природным минералом и может с успехом заменить промышленные марки сорбентов. Эффективность катионита при селективном извлечении ионов исследуемого металла позволяет проводить сорбцию из растворов, содержащих примесные ионы цветных металлов.
Библиографическая ссылка
Ергожин Е.Е., Акимбаева А.М., Товасаров А.Д. ОРГАНОМИНЕРАЛЬНЫЙ КАТИОНИТ НА ОСНОВЕ ПРИРОДНОГО БЕНТОНИТА // Современные наукоемкие технологии. 2005. № 10. С. 81-82;URL: https://top-technologies.ru/ru/article/view?id=23685 (дата обращения: 29.04.2026).



