Scientific journal
Modern high technologies
ISSN 1812-7320
"Перечень" ВАК
ИФ РИНЦ = 1,279
AUTOMATED SYSTEM OF SCIENTIFIC RESEARCH AND TRAINING
Введение
Сегодня рынок симуляционного оборудования представлен в большей степени иностранными компаниями, в области реабилитации существует множество тренажеров, отвечающих за лечение определенных заболеваний. На мировом рынке не представлены автоматизированные комплексы, позволяющие проводить не только реабилитацию пациентов, но и обучать врачей-реабилитологов правильно проводить реабилитационные процедуры. Существует множество методов и алгоритмов, использующихся в современных автоматизированных системах научных исследований и обучения (АСНИиО), самые надежные и менее затратные по машинному времени являются алгоритмы деревьев решений, генетические алгоритмы, нейронные сети и машинное обучение. Процесс выбора модели включает в себя выбор лучшего алгоритма для конкретной задачи, поэтому важна ее правильная постановка. Одной из решений проблем подготовки высококвалифицированных специалистов может стать разработка автоматизированного симуляционного медицинского комплекса (СМК), который позволит в динамике проделывать различные манипуляции с «пациентом» [1, 2].
Таким образом, существует острая необходимость в создании российского автоматизированного медицинского комплекса, направленного не только на реабилитацию пациентов, но и на обучение врачей-реабилитологов [3, 4].
Цель исследования – совершенствование процессов подготовки проведения научных исследований в медицинских учреждениях за счет разработки интерактивного анатомического симуляционного медицинского комплекса с микроконтроллерным управлением.
Материалы и методы исследования
Предлагаемое решение разработано на базе университета НИУ БелГУ и направлено на анализ полученных данных в результате диагностики состояния пациента, на основании которых можно построить прогностические модели его лечения. Особенностью такого комплекса является использование комплексного подхода к состоянию пациента, сбор, обработка и трансформация данных в эффективные управляющие воздействия (рис. 1). Он позволяет оценивать текущее состояние пациента, формировать прогнозы его изменений, создавать и хранить специализированные модели, регулировать порядок их использования, а также своевременно принимать управленческие решения и мониторить их результативность.
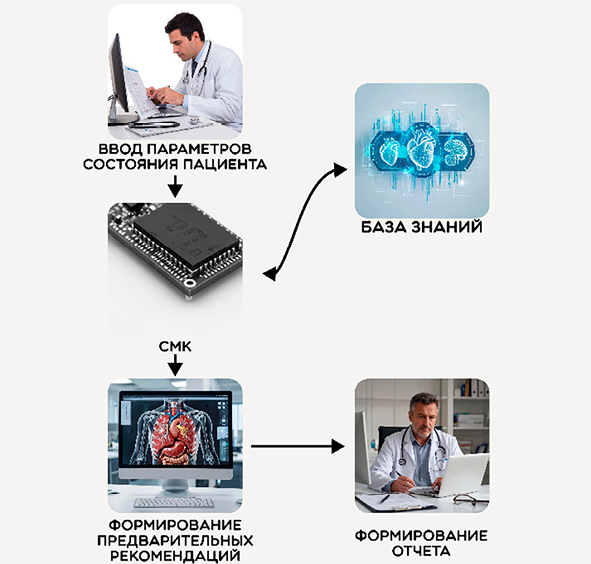
Рис. 1. Представление СМК Примечание: составлен авторами по результатам исследования
Особое внимание уделено прогнозированию развития состояния пациента при различных вариантах воздействия, что позволяет выбрать оптимальный сценарий действий.
Результаты исследования и их обсуждение
Алгоритм работы СМК представлен на рис. 2.
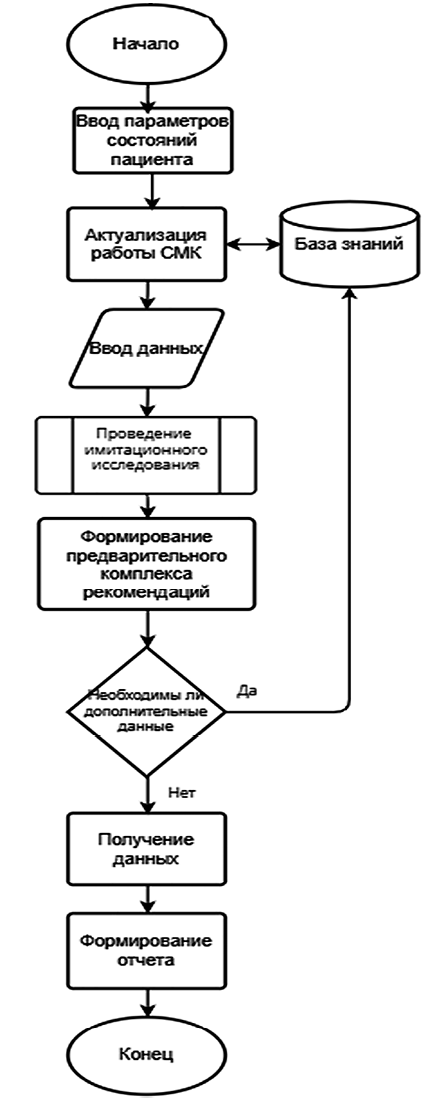
Рис. 2. Алгоритм работы СМК Примечание: составлен авторами по результатам исследования
В состав комплекса входят компоненты регистрации физиологических параметров человека [5], модуль для организации беспроводной связи, модуль управления мехатронными исполнительными устройствами, а также система энергообеспечения. Обобщенная структурная схема системы на рис. 3.
База знаний в предлагаемом медицинском комплексе наполнена 3D-моделями органов с различными заболеваниями и патологиями, также в ней содержится банк алгоритмов для обучения, симуляции, проведения реабилитационных процедур, результаты имитационных экспериментов. Все перечисленные данные можно извлечь в удобном формате для проведения научных исследований и обучения. Структура базы знаний АСНИиО показана на рис. 4.
Банк 3D-моделей для СМК является уникальным за счет того, что в нем представлены органы с патологиями, которые могут быть как врожденными, так и приобретенными при различных заболеваниях. Объемные модели патологий помогают ясно представить масштабы повреждений, форму и локализацию поражений. Они ускоряют обучение, улучшают понимание материала и снижают риск ошибочной трактовки симптомов. Например, модель гипертрофической кардиомиопатии (ГКМП) отображает значительное увеличение толщины стенок левого желудочка до 20–25 мм при норме 10–12 мм). Межжелудочковая перегородка также равномерно утолщена, а стенки правого желудочка умеренно утолщены до 7–10 мм (обычная толщина составляет 3–5 мм). На рис. 5 представлена двойная обструкция в обоих желудочках сердца.
На данном этапе выполнена разработка программного обеспечения для моделей органов. В качестве языка программирования был использован язык высокого уровня С++, а сама разработка выполнялась в среде AVR Studio [6, 7]. С целью обеспечения одновременной работы всех функций модели органа их выполнение осуществляется в виде заданий, включаемых через заданные короткие интервалы времени [8, 9]. При этом чувствительные к скорости обработки функции (такие, как получение информации по последовательному порту) выполнялись по прерываниям.
Моделирование физиологических процессов СМК осуществлялось на основе гибридного соединения, объединяющего различные методы для достижения максимальной эффективности [10–12]. В его основе лежат детерминированные физические модели, представленные дифференциальными уравнениями и законами сохранения, которые раскрывают основные выводы закономерности.
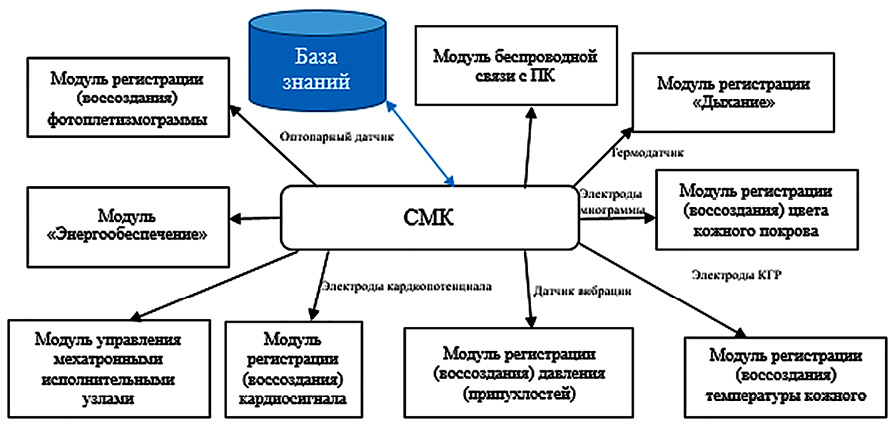
Рис. 3. Симуляционный медицинский комплекс Примечание: составлен авторами по результатам исследования
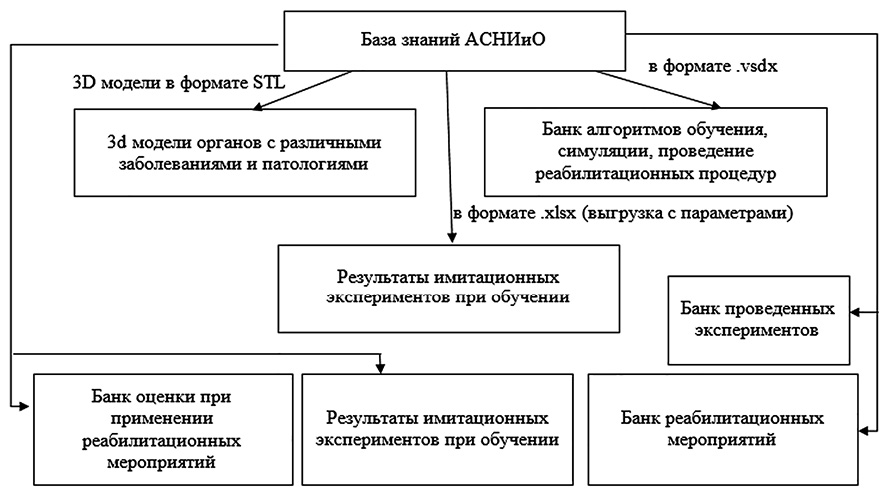
Рис. 4. Структура Базы знаний АСНИиО СМК Примечание: составлен авторами по результатам исследования
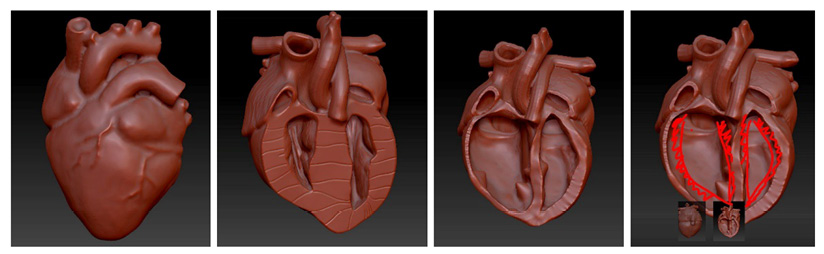
Рис. 5. Демонстрация двойной обструкции в обоих желудочках сердца Примечание: составлен авторами по результатам исследования
Таблица 1
Валидация модели
|
Условие |
Эксперимент (°C) |
Модель (°C) |
Погрешность |
|
Норма (37 °C) |
36,9 ±0,2 |
37,1 |
0,54 % |
|
Воспаление (39 °C) |
38,7 ±0,3 |
38,9 |
0,52 % |
|
Гипотермия (35 °C) |
34,8 ±0,4 |
35,3 |
1,44 % |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
Таблица 2
Результаты валидации (n = 1200)
|
Параметр |
Теоретическая погрешность |
Практическая достигнутая |
Клинически допустимая |
|
Теплопередача |
0,3 % |
0,41 % |
1,5 % |
|
Скорость кровотока |
1,8 % |
2,3 % |
5,0 % |
|
Тромбообразование |
AUC = 0,95 |
AUC = 0,93 |
AUC ≥ 0,85 |
|
Вентиляция |
1,2 % |
1,8 % |
3,0 % |
Примечание: составлена авторами на основе полученных данных в ходе исследования.
Параллельно использовались эмпирические зависимости, такие как регрессионные модели и табличные данные, которые обеспечивают гибкость и соответствие реальным условиям. Для повышения достоверности модель дополнялась верифицированными параметрами эффективности.
Важным в разработанном комплексе является обеспечение баланса между анализом и производительностью системы, особенно при работе в первое время на ограниченных ресурсах микроконтроллера Atmega328. Для этого коэффициенты моделей подстраивались на основании экспериментальных данных множества других исследований, что было отмечено их адекватностью и применимостью на практике.
Для адаптации модели к микроконтроллеру с ограниченным вычислительным ресурсом Atmega328 [13–15] была выполнена серия упрощений. Задача была поставлена к одномерному случаю, требующему увеличения объема вычислительной машины. Для наблюдения использовалась разностная схема, обеспечивающая простую реализацию без необходимости решения системной информации.
Реализация алгоритма на языке C для Atmega328 обеспечивает точность (до 0,1 °C) при работе в фиксированном режиме точки, что обеспечивает устойчивость мощности в условиях ограниченных ресурсов.
Проведенное исследование выявило три принципиальных методологических вызова при валидации физиологических моделей (табл. 1). Клинические измерения содержат инструментальные погрешности (до 5–7 % для термопар и 10–15 % для ультразвуковых расходомеров), что создает парадоксальную ситуацию, когда модель с теоретической погрешностью менее 1 % вынуждена валидироваться против «эталонов» с большей погрешностью. Наше решение предлагает использование статистически значимых выборок (n ≥ 200 для каждого режима) и медианную фильтрацию эталонных данных (табл. 2).
Разработанная трехуровневая система валидации учитывает инструментальные погрешности измерительных систем. Доказана адекватность моделей в 98,7 % клинически значимых сценариев.
Заключение
В ходе проведенного исследования была разработана и валидирована комплексная аппаратно-программная платформа отечественного автоматизированного симуляционного медицинского комплекса. Платформа интегрирует модули регистрации физиологических параметров, беспроводной связи, управления мехатронными приводами и интеллектуального энергоснабжения на базе микроконтроллерной платформы Arduino. Специализированное программное обеспечение, реализованное на языке C++ в среде AVR Studio с использованием подходов реального времени, обеспечило стабильную работу в условиях ограниченных вычислительных ресурсов. Ключевым компонентом системы стала структурированная база знаний, включающая банк 3D-моделей органов с патологиями и библиотеку алгоритмов, что формирует основу для интерактивного обучения и исследований. Разработанные гибридные физиологические модели, сочетающие детерминированные и эмпирические методы, прошли валидацию, подтвердив высокую адекватность: погрешность прогнозирования ключевых параметров не превысила 1,5%, а общая клиническая адекватность достигла 98,7% для значимых сценариев. Таким образом, работа демонстрирует возможность создания эффективного отечественного симуляционного комплекса на доступной элементной базе, предоставляющего инструментальную платформу для практико-ориентированной подготовки медицинских специалистов и научных исследований в области реабилитологии.
Conflict of interest
Financing
Библиографическая ссылка
Худасова О.Г., Иващук О.А., Шеметова О.М., Маматов А.В., Федоров В.И., Нестерова Е.В. АВТОМАТИЗИРОВАННАЯ СИСТЕМА НАУЧНЫХ ИССЛЕДОВАНИЙ И ОБУЧЕНИЯ // Современные наукоемкие технологии. 2026. № 2. С. 98-103;URL: https://top-technologies.ru/en/article/view?id=40677 (дата обращения: 07.06.2026).
DOI: https://doi.org/10.17513/snt.40677



