Scientific journal
Modern high technologies
ISSN 1812-7320
"Перечень" ВАК
ИФ РИНЦ = 1,279
DEVELOPMENT OF A THREE-DIMENSIONAL COMPUTER MODEL OF THE HUMAN MEDIASTINUM FOR ELECTRICAL IMPEDANCE TOMOGRAPHY
Введение
Решение научно-технических задач электроимпедансной томографии (ЭИТ) [1; 2] требует получения измерительной информации с исследуемого объекта для дальнейшей реконструкции и визуализации поля проводимости. Этого можно достичь двумя способами –использовать аппаратно-программные комплексы ЭИТ или компьютерные модели объекта исследования. Очевидно, что наиболее подходящим и верным является проведение физического эксперимента с применением ЭИТ-томографа. Однако это требует разработки и изготовления самого устройства, т.к. в свободном доступе отсутствуют изделия на основе ЭИТ (в том числе и коммерческие), которые можно использовать в научно-исследовательских целях. Таким образом, использование средств математического и компьютерного моделирования является практически единственным и востребованным инструментом для выполнения широкого спектра исследований для задач ЭИТ.
Следует отметить, что наибольшее распространение метод ЭИТ получил для мониторинга глобальных и регионарных параметров системы внешнего дыхания человека. Среди значимых направлений клинического применения ЭИТ можно выделить мониторинг процессов вентиляции и перфузии легких [3] на основе оценки изменения реконструированного поля проводимости (или изменений поля проводимости) в заданном сечении, определяемом плоскостью наложения электродной системы (ЭС) на теле пациента, в том числе находящегося на респираторной поддержке или подключенного к аппарату искусственной вентиляции легких (ИВЛ). Данное направление в настоящее время активно развивается и требует разработки новых инструментов для выполнения прикладных научных исследований, направленных на изучение возможностей метода ЭИТ. При этом является актуальным решение проблем получения и обработки первичной измерительной информации, необходимой для разработки специализированного алгоритмического и методического обеспечения ЭИТ. Для решения подобного рода задач ЭИТ в мировой практике широко распространены подходы, основанные на использовании компьютерных моделей, разрабатываемых под конкретные задачи [4-6]. При этом анализ развития данной области показывает, что перспективным направлением является разработка не просто упрощённых конечно-элементных моделей для двумерной или трехмерной ЭИТ легких человека, а моделей, содержащих набор внутренних структур в исследуемой области, имеющих сложную геометрию, позволяющих моделировать получение первичной измерительной информации для заданной патологии при различных конфигурациях ЭС. В этой связи, с учетом полученного опыта ранее выполненных научных и инженерных изысканий, а также анализа современного состояния исследований в мировой практике в области ЭИТ легких человека, авторами предложено разработать многокомпонентную модель средостения человека в среде COMSOL Multiphysics [7-9]. Выбор данного специализированного программного обеспечения обусловлен тем, что, в отличие от EIDORS [10], параметры модели могут быть заданы непосредственно в программе, включая геометрию объекта, состав и электрические свойства тканей, конфигурацию электродов и алгоритмы инжектирования тока и измерения. Это позволит значительно сократить время и ресурсы, затрачиваемые на подготовку к проведению исследовательских испытаний, и расширить номенклатуру потенциально возможных решаемых задач ЭИТ. На первом этапе планируется оценить возможность получения измерительной информации (решение прямой задачи ЭИТ) [11].
Целью данного исследования являлась разработка компьютерных моделей в среде COMSOL Multiphysics для решения прямой задачи ЭИТ при моделировании патологий дыхания, которые могут возникнуть при ИВЛ. Для достижения указанной цели ставились и решались следующие задачи:
1) в программе Blender 3D разработать геометрию органов средостения человека, включающую в себя легкие, сердце, ребра, позвоночник, мышечную ткань и кожу, позволяющую обеспечить высокое совпадение пропорций и форм органов с реальными, для дальнейшего моделирования нарушений системы внешнего дыхания;
2) экспортировать геометрию органов средостения человека в формат STL и импортировать в среду COMSOL Multiphysics, что позволит разработать для каждой 3D-модели органов средостения конечно-элементные объекты (внутренние структуры);
3) объединить конечно-элементные объекты органов средостения в единую компьютерную модель, где учтены электрические свойства тканей (диэлектрическая проницаемость и проводимость) для проведения дальнейшего корректного моделирования;
4) на геометрии средостения человека расположить электроды ЭС, сформированные как идеально проводящие материалы с нулевым сопротивлением с возможностью модернизации в будущем конфигурации ЭС и геометрических размеров электродов, в том числе замены на другие формы;
5) запустить процесс моделирования нормального состояния легких и патологий (заполнение части легкого жидкостью, уменьшение эффективной емкости легких) системы внешнего дыхания человека;
6) решить прямую задачу ЭИТ и получить распределение изменений потенциалов в плоскости наложения ЭС для моделей без патологий и с нарушениями с использованием круглых электродов;
7) дать оценку полученным результатам.
Материалы и методы исследования
Для моделирования ЭИТ-исследования реализован алгоритм, изображенный на рисунке 1.
Создание геометрии 3D-модели средостения человека выполнялось в программе Blender 3D. Модель разработана на основе анатомических данных [12] и обеспечивает максимальное соответствие реальным пропорциям и форме органов. Средостение представлено как единая геометрическая структура, внутри которой выделены отдельные области для легких, сердца, ребер и части позвоночного столба, мышечной ткани и кожи. Импорт модели в COMSOL Multiphysics осуществлялся с использованием встроенных инструментов для работы с внешними геометрическими данными.
В качестве аппаратного обеспечения использовалась виртуальная машина с основными параметрами, приведенными в таблице 1.
Для выполнения испытаний на базе предложенных моделей разработано специализированное алгоритмическое и программное обеспечение, обеспечивающее автоматизацию исследования, а также управление режимами и параметрами моделирования.
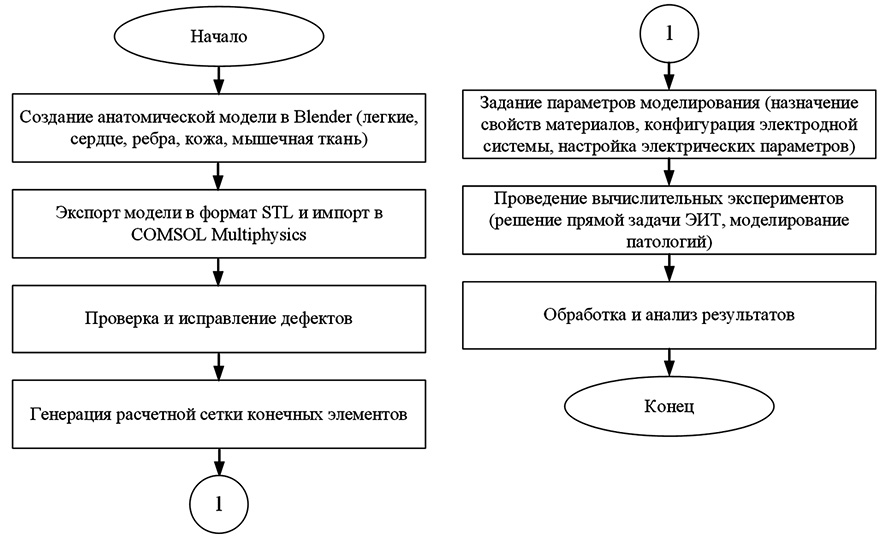
Рис. 1. Блок-схема алгоритма проведения экспериментальных исследований Примечание: составлено авторами по результатам данного исследования
Таблица 1
Параметры, используемые при обработке полученных данных
|
№ п/п |
Параметр |
Значение |
|
1 |
Процессор, ГГц |
Intel Xeon E5-2680-v3 @ 2.5 ГГц |
|
2 |
ОЗУ, ГБ |
38 |
|
3 |
Операционная система |
Windows 10 |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Таблица 2
Параметры ЭИТ, задаваемые при моделировании
|
№ п/п |
Параметр |
Значение |
|
1 |
Частота инжектируемого тока (f), кГц |
20 |
|
2 |
Амплитуда инжектируемого тока (I), мА |
5 |
|
3 |
Количество электродов, шт. |
16, ряд 1 |
|
4 |
Форма тока |
Синусоидальный |
|
5 |
Протокол сбора данных ЭИТ |
«Ближайший сосед» |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Таблица 3
Параметры конструкции электродной системы ЭИТ, использованные в ходе моделирования
|
№ п/п |
Параметр |
Значение |
|
1 |
Число электродов, шт. |
16 |
|
2 |
Число поясов, шт. |
4 |
|
3 |
Форма |
круг |
|
4 |
Диаметр, мм |
19 |
|
5 |
Среднеквадратичное отклонение расстояния между электродами, мм |
0 (равноудаленные электроды) |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Исследования (решение прямой задачи ЭИТ) выполнены для следующих состояний легких: а) модель без патологий, полный вдох; б) модель без патологий, полный выдох; в) заполнение части легкого жидкостью, полный вдох; г) заполнение части легкого жидкостью, полный выдох; д) уменьшение эффективной емкости легких, полный вдох; е) уменьшение эффективной емкости легких, полный выдох.
Электроды, задаваемые в модели, представляют собой идеально проводящие материалы с нулевым сопротивлением и равномерно распределены по поверхности средостения. При разработке модели изначально заложено использование электродов круглой и прямоугольной форм, однако исследований второго типа в рамках настоящей работы не выполнено (подобные испытания являются предметом дальнейших исследований). Прямоугольные имеют размер 32×22 мм, а круглые – диаметр 19 мм. Выбор непосредственно круглых электродов в рамках настоящих исследований обусловлен публикациями [13; 14], в которых показана их перспективность применения на практике.
В таблице 2 приведены параметры ЭИТ, задаваемые при моделировании.
В исследовании применялась конструкция электродной системы ЭИТ, параметры которой указаны в таблице 3.
В ходе моделирования объем первичной измерительной информации, получаемой при решении прямой задачи ЭИТ, составил 9.5 Мб.
Результаты исследования и их обсуждение
Пример разработки моделей органов средостения человека в Blender 3D приведен на рисунке 2. Для упрощения моделирования в COMSOL Multiphysics модель оптимизирована с учетом требований к сетке и геометрической совместимости.
После завершения моделирования в Blender 3D полученная 3D-модель экспортирована в формат STL. Импорт модели в COMSOL Multiphysics осуществляется с использованием встроенных инструментов для работы с внешними геометрическими данными. Интерфейс программы с моделью средостения приведен на рисунке 3.
В ходе выполнения алгоритмических действий по импорту модели в COMSOL Multiphysics осуществляется проверка на наличие ошибок (пересечения поверхностей или незамкнутые области), среди которых имеют место быть дефекты, такие как небольшие отверстия или проблемы пересечения границ объектов. После устранения возникающих неточностей геометрия готова для разбиения на конечные элементы [15].
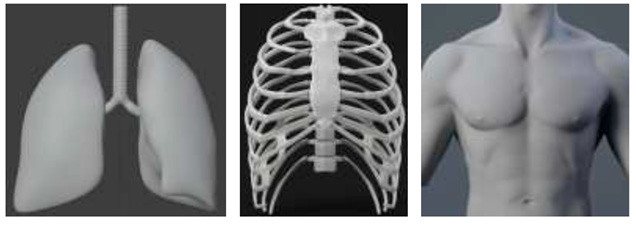
Рис. 2. Разработка моделей органов средостения человека в Blender 3D Примечание: составлено авторами по результатам данного исследования
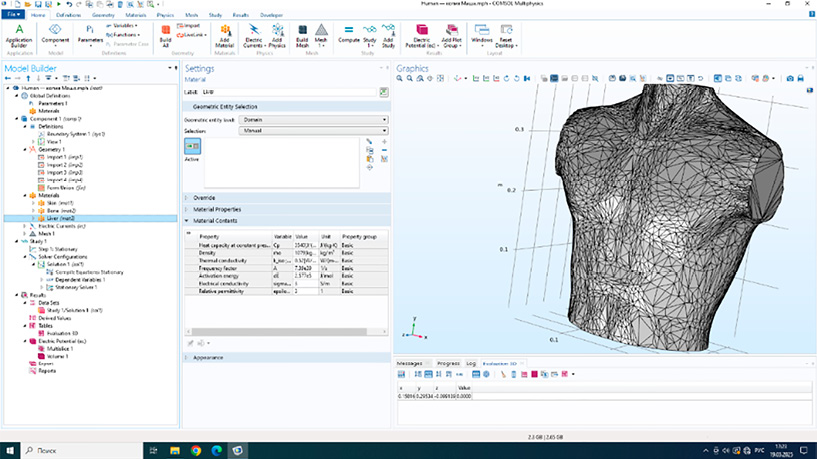
Рис. 3. Интерфейс программы COMSOL Multiphysics Примечание: составлено авторами по результатам данного исследования
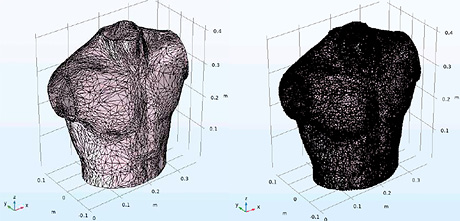
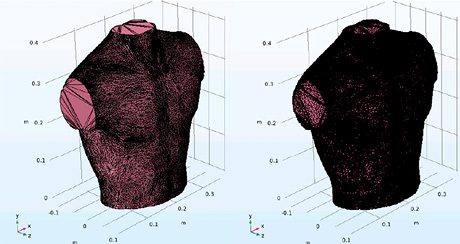
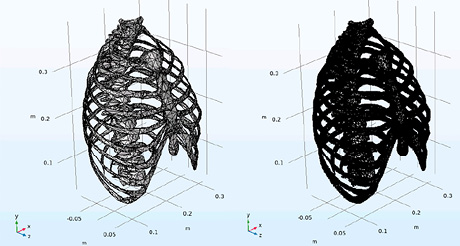
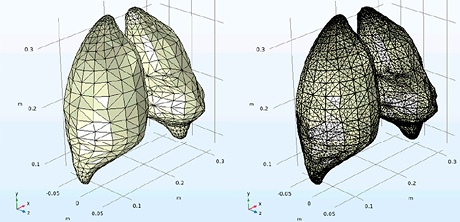
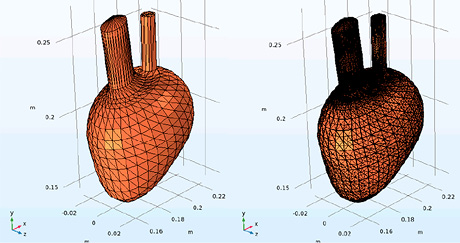
Для объектов (т.е. моделей объектов), входящих в состав средостения, наиболее подходящей является тетраэдральная сетка, так как она позволяет аппроксимировать сложные анатомические структуры. Далее настраиваются параметры сетки и выполняется ее генерация с дальнейшей проверкой ее на равномерность распределения элементов и отсутствие искажений. При обнаружении проблем (например, несоответствие геометрии элементов в определенных областях) выполняется локальное измельчение или изменение параметров сетки. В таблице 4 приведены результаты разработки трехмерных конечно-элементных моделей органов средостения человека.
В таблице 5 представлены электрические параметры, использованные при моделировании.
Далее выполняется задание числа электродов в программе и задается их распределение по поверхности средостения. В базовой версии модели заданы два типа геометрии электродов – круглые и прямоугольные металлические электроды. Оба типа электродов представляют собой идеально проводящие материалы с нулевым сопротивлением и равномерно распределены по поверхности средостения, что отражает реальное расположение ЭС на теле пациента, позволяющее уменьшить число артефактов на реконструированном и визуализированном поле изменения проводимости.
В предложенной модели предусмотрено создание максимально возможного количества электродов, а регулирование их числа фактически реализуется за счет выбора уже используемых. Изменение конструкции ЭС реализуется следующим образом: создаются несколько моделей с различными конфигурациями электродного ряда, и в зависимости от выбора пользователя применяется один из них. Данные принципы поясняют рисунок 4.
Таблица 4
Трехмерные конечно-элементные модели органов средостения человека
|
Орган |
Геометрическая модель |
Результат разбиения на конечные элементы |
|
Кожа |
|
|
|
Мышечная ткань |
|
|
|
Ребра и часть позвоночного столба |
|
|
|
Легкие |
|
|
|
Сердце |
|
|
Примечание: составлено авторами на основе полученных данных в ходе исследования.
аблица 5
Электрические параметры отдельных органов средостения, использованные при моделировании
|
№ п/п |
Орган |
Диэлектрическая проницаемость, о.е. |
Электрическая проводимость, См/м |
Примечания |
|
1 |
Кость № 1 |
1.53Е+1 |
6.43Е-2 |
- |
|
2 |
Кость № 2 |
2.67Е+1 |
1.73Е-1 |
Раковая опухоль |
|
3 |
Бронхи |
1.00Е+0 |
0.00Е-1 |
Во время вдоха |
|
4 |
Мышцы |
6.60Е+1 |
7.08Е-1 |
- |
|
5 |
Сердечная мышца |
9.08Е+1 |
7.33Е-1 |
- |
|
6 |
Печень |
6.90Е+1 |
4.87Е-1 |
- |
|
7 |
Легкие № 1 |
3.16Е+1 |
3.06Е-1 |
Во время вдоха |
|
8 |
Легкие № 2 |
6.71Е+1 |
5.59Е-1 |
Во время выдоха |
|
9 |
Кожа |
7.29Е+1 |
4.91Е-1 |
Влажная |
|
10 |
Кровь |
7.68Е+1 |
1.23Е+0 |
- |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
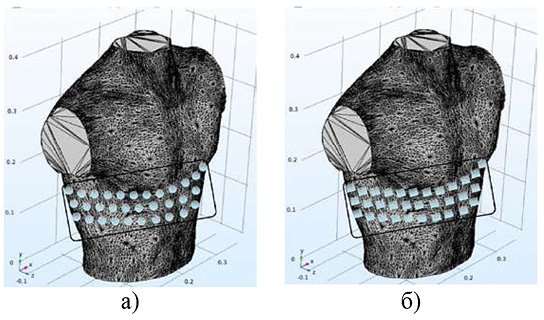
Рис. 4. Трехмерная конечно-элементная модель средостения человека с вариантами размещения электродов: а – использование круглых электродов; б – использование электродов прямоугольной формы (данный функционал реализован, но не исследуется в статье) Примечание: составлено авторами по результатам данного исследования
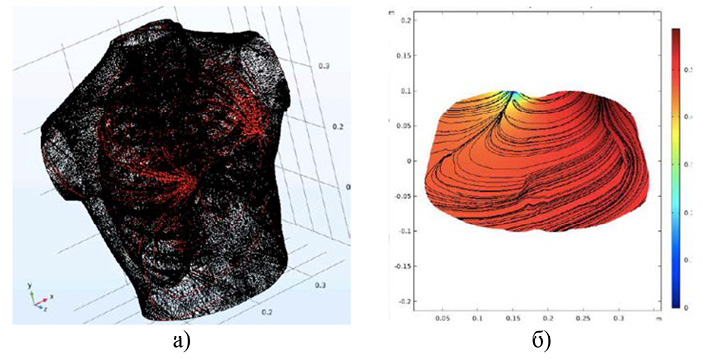
Рис. 5. Трехмерная конечно-элементная модель средостения человека в условиях отсутствия патологий: а – потенциальные линии плотности тока; б – результат оценки распределения электрического потенциала φ и линий плотности тока в сечении на уровне 20 см Примечание: составлено авторами по результатам данного исследования
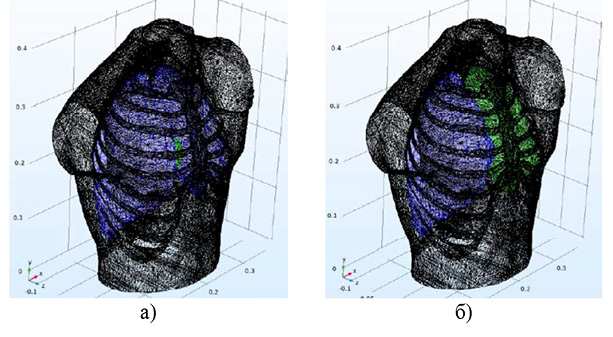
Рис. 6. Трехмерная конечно-элементная модель торса человека в условиях наличия патологий: а – заполнение части легкого жидкостью (малая область в центре, выделена зеленым цветом); б – уменьшение эффективной емкости левого легкого Примечание: составлено авторами по результатам данного исследования
Таблица 6
Пример первичных данных ∆φ исследовательских испытаний для круглых электродов
|
Модель без патологий, полный вдох |
Модель без патологий, полный выдох |
Заполнение части легкого жидкостью, полный вдох |
Заполнение части легкого жидкостью, полный выдох |
Уменьшение эффективной емкости легких, полный вдох |
Уменьшение эффективной емкости легких, полный выдох |
|
0,033 |
0,014 |
-0,322 |
-0,159 |
-0,362 |
-0,222 |
|
-0,021 |
-0,005 |
-0,141 |
-0,122 |
-0,083 |
-0,051 |
|
-0,052 |
-0,015 |
0,048 |
0,082 |
0,099 |
0,064 |
|
-0,011 |
-0,005 |
0,087 |
0,013 |
-0,059 |
-0,043 |
|
-0,044 |
-0,011 |
-0,019 |
-0,031 |
0,107 |
0,071 |
|
-0,054 |
-0,015 |
0,089 |
0,072 |
0,075 |
0,056 |
|
-0,027 |
-0,012 |
0,117 |
0,085 |
0,059 |
0,047 |
|
0,046 |
0,015 |
-0,061 |
0,011 |
-0,026 |
-0,026 |
|
0,011 |
0,005 |
0,067 |
0,015 |
0,061 |
0,046 |
|
0,069 |
0,024 |
0,023 |
0,027 |
-0,054 |
-0,038 |
|
… |
… |
… |
… |
… |
… |
Примечание: составлено авторами на основе полученных данных в ходе исследования.
Результаты трехмерного конечно-элементного моделирования в условиях отсутствия патологий при частоте инжектирующего тока 20 кГц показаны на рисунке 5.
На рисунке 6 показаны результаты трехмерного моделирования (при частоте инжектирующего тока 20 кГц) в условиях наличия патологий, которые могут произойти при искусственной вентиляции легких [16; 17], а именно:
1) заполнение части легкого жидкостью, что соответствует появлению статической локальной зоны с повышенной внутренней электрической проводимостью σ на общей картине поля проводимостей;
2) уменьшение эффективной емкости легких, что соответствует уменьшению максимального размера зоны пониженной внутренней электрической проводимости σ на общей картине поля проводимостей.
Проведены измерения изменения (разности) потенциалов ∆φ (мВ) на всех круглых электродах при различных конфигурациях инжектирования тока и изменения ∆φ (использован протокол сбора данных ЭИТ «Ближайший сосед»).
Структурирование данной информации в виде таблиц занимает огромный объем страниц, поэтому для примера в таблице 6 представлен набор первичной измерительной информации при испытании возможности задания числа электродов для минимального значения (16 шт.) – форма круг.
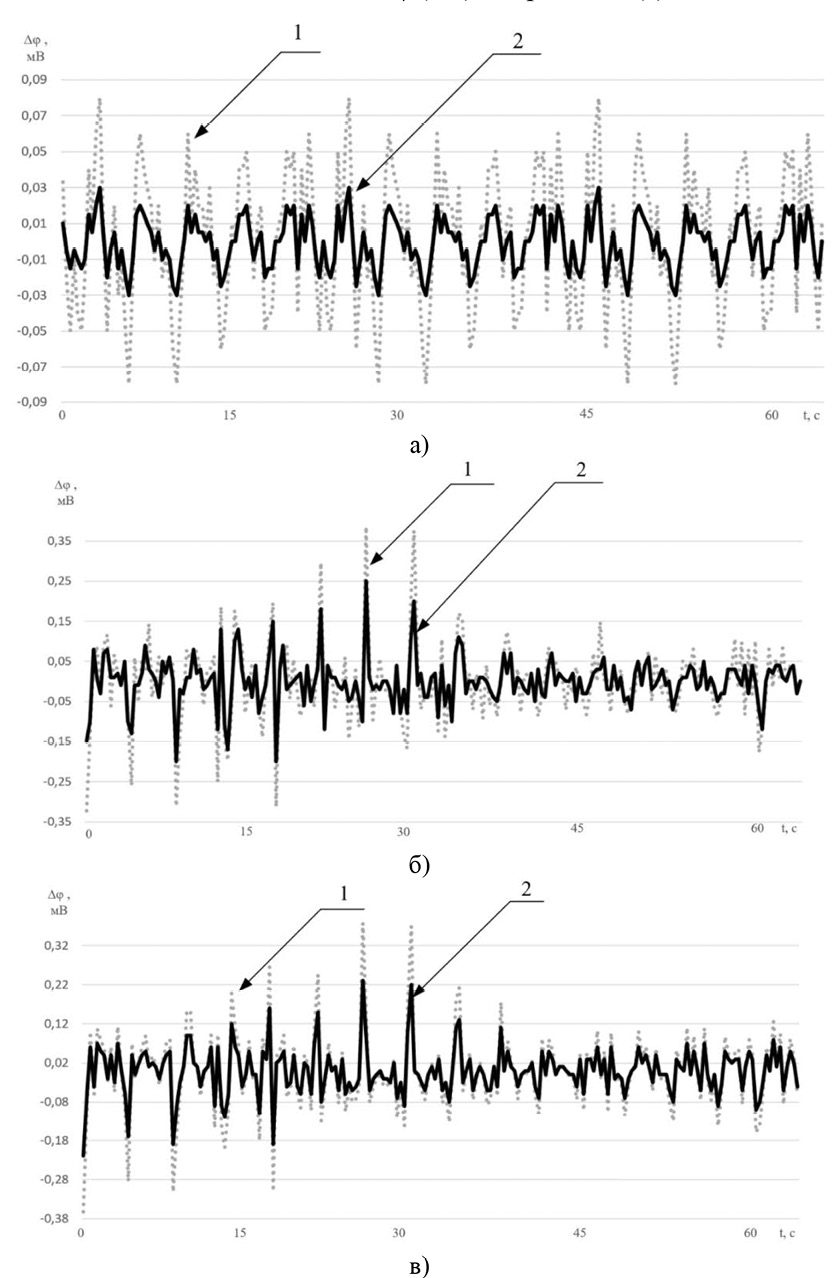
Рис. 7. Результаты исследовательских испытаний для круглых электродов: а – модель без патологий; б – заполнение части легкого жидкостью; в – уменьшение эффективной емкости легких Примечание: составлено авторами по результатам данного исследования
При использовании 32-электродной системы ЭИТ число строк увеличится с 208 до 928. При испытании возможности задания числа электродов для минимального значения числа электродов формируется 16 подобных таблиц.
Следует пояснить, что круглые электроды выбраны, так как обеспечивают радиально-симметричное распределение электрического поля, равномерное давление на ткань и лучший контакт с неровными поверхностями тела. Прямоугольные электроды демонстрируют выраженные краевые эффекты, зависимость результатов от ориентации, неравномерность контактного давления, поэтому для формы электродов в виде прямоугольника исследования в данной работе не проводились. В дальнейшем планируется проведение исследований на прямоугольных электродах для сравнения данных и оценки влияния формы электродов на измерения в ЭИТ.
На рисунке 7 приведены результаты исследовательских испытаний для круглых электродов, приведенные на графиках для модели без и с наличием патологий для полного вдоха (с максимальной проводимостью ∆φ) – показан цифрой 1, и полного выдоха (с минимальной проводимостью ∆φ) – показан цифрой 2. На графиках представлена зависимость значения изменения потенциалов ∆φ (мВ) от времени t (с).
Следует отметить, что, несмотря на полученные результаты, одним из возможных источников ошибок является упрощение геометрии модели. Некоторые анатомические особенности, такие как мелкие кровеносные сосуды или неровности поверхности тканей, не учтены. Это может привести к незначительным отклонениям в распределении потенциалов. Другим источником ошибок является задание электрических свойств тканей. В реальных условиях электропроводность тканей может варьироваться в зависимости от физиологического состояния [16-18], что не всегда учитывается в модели. Несмотря на эти ограничения, результаты моделирования демонстрируют соответствие теоретическим ожиданиям и могут быть использованы для решения задач по моделированию патологий легких, оптимизации размеров электродов и конструкции ЭС в устройствах ЭИТ.
В рамках анализа современного состояния исследований в области ЭИТ следует, что прямые аналоги представленной в статье комплексной трёхмерной модели человеческого средостения, созданной по технологии моделирования в Blender 3D и дальнейшем задании электрофизических параметров в COMSOL Multiphysics, в доступной научной литературе отсутствуют. Проведённый поиск показывает, что большинство работ по трёхмерному моделированию сосредоточено в области обработки медицинских изображений с применением машинного обучения [19]. Эти методы принципиально отличаются от цели настоящего исследования, которое заключается не в анализе готовых снимков, а в создании анатомически детализированной геометрической модели с нуля для решения прямой задачи ЭИТ.
Новизна текущей работы заключается в комплексности подхода и уровне анатомической детализации. В отличие от известных аналогов, которые часто фокусируются на упрощённых геометриях или ограниченном наборе органов, разработанная модель включает в единую структуру легкие, сердце, ребра, позвоночник, мышечные ткани и кожу. Исследование также направлено на модульность и гибкость конфигурации электродной системы с возможностью вариации формы, размера и расположения электродов, что позволяет оптимизировать аппаратную часть ЭИТ-систем [20; 21]. Коллективом авторов ранее проводились разработки по применению COMSOL Multiphysics для моделирования процессов ЭИТ [8] и созданию методик мониторинга дыхательной системы [18], однако эти исследования базировались на более простых моделях.
Выводы
Проведенные исследования и разработки позволили создать масштабируемый программный инструментарий для выполнения широкого спектра работ в области ЭИТ легких человека, в том числе для задач моделирования патологий, которые могут возникнуть при ИВЛ. К основным результатам, полученным в рамках данной статьи, можно отнести следующее:
1) в программе Blender 3D разработана геометрия органов средостения человека, включающая в себя легкие, сердце, ребра, позвоночник, мышечную ткань и кожу, позволяющая обеспечить высокое совпадение пропорций и форм органов с реальными, для дальнейшего моделирования нарушений системы внешнего дыхания;
2) полученная геометрия органов средостения человека переведена в формат STL и импортирована в среду COMSOL Multiphysics, это позволило разработать для каждой 3D-модели органов средостения конечно-элементные объекты (внутренние структуры), что сократило время на разработку многокомпонентной модели средостения;
3) конечно-элементные объекты органов средостения объединены в единую компьютерную модель, где учтены электрические свойства тканей (диэлектрическая проницаемость и проводимость) для проведения дальнейшего корректного моделирования. Тем самым разработана и апробирована методика построения модели средостения человека для задач ЭИТ с использованием справочной анатомической информации;
4) на геометрии средостения человека расположены электроды ЭС, сформированные как идеально проводящие материалы с нулевым сопротивлением с возможностью модернизации в будущем конфигурации ЭС и геометрических размеров электродов, в том числе замены на другие формы. Это позволяет значительно расширить потенциальные направления исследований ЭИТ легких человека в части разработки оптимальных конфигураций ЭС, а также предложить иные способы схемы первичной измерительной информации;
5) выполнен процесс моделирования нормального состояния легких и патологий (заполнение части легкого жидкостью, уменьшение эффективной емкости легких) системы внешнего дыхания человека, результаты которого подтвердили возможность применения предложенного инструментария для решения прямой задачи ЭИТ;
6) решена прямая задача ЭИТ и получено распределение изменений потенциалов в плоскости наложения ЭС для моделей без патологий и с нарушениями с использованием круглых электродов.
В краткосрочной перспективе планируется проведение исследований на прямоугольных электродах для сравнения данных и оценки влияния формы электродов на измерения в ЭИТ. Перспективным направлением является использование других форм электродов, например прямоугольных, а также доработка модели в части дальнейшей детализации внутренних структур органов средостения человека. Кроме того, полученная модель может быть доработана для выполнения мультифизического моделирования, поскольку среда COMSOL Multiphysics является эффективным инструментом для решения многодисциплинарных задач, что особенно важно для ЭИТ, где необходимо учитывать взаимодействие электрических полей с биологическими тканями.
Conflict of interest
Financing
Библиографическая ссылка
Конько М.А., Алексанян Г.К., Темняков Н.С., Набиулин Е.А. РАЗРАБОТКА ТРЕХМЕРНОЙ КОМПЬЮТЕРНОЙ МОДЕЛИ СРЕДОСТЕНИЯ ЧЕЛОВЕКА ДЛЯ ЭЛЕКТРОИМПЕДАНСНОЙ ТОМОГРАФИИ // Современные наукоемкие технологии. 2025. № 12. С. 89-100;URL: https://top-technologies.ru/en/article/view?id=40609 (дата обращения: 08.06.2026).
DOI: https://doi.org/10.17513/snt.40609