Scientific journal
Modern high technologies
ISSN 1812-7320
"Перечень" ВАК
ИФ РИНЦ = 1,279
THE INCREASE IN YIELD OF HUMIC SUBSTANCES FROM BROWN COAL OF KHARANOR DEPOSIT BY DIRECTED OXIDATION
В последние годы произошло резкое падение объемов добычи бурых углей вследствие их низкой конкурентоспособности как энергоносителей. Назрела необходимость поиска альтернативных и эффективных методов их использования. В связи с этим все чаще поднимается вопрос глубокой переработки этого вида сырья и создание на основе месторождений бурых углей сырьевой базы для углехимической промышленности [5]. Одним из методов, позволяющих не только расширить условия процессов переработки углей, но и получить продукты с более разнообразными свойствами, является окисление.
Окисление твердых горючих ископаемых, как химический процесс, можно рассматривать с двух позиций: самопроизвольное окисление (автоокисление) и направленное окисление. Окисленный уголь – это форма твердого углерода, содержащая на своей поверхности кислородсодержащие функциональные группы. Автоокисление протекает в естественных условиях в пластах, при хранении на складах, при транспортировке. В данном случае окисление является нежелательным процессом, поскольку снижает качество углей. Направленное окисление является основой переработки углей с получением полезных продуктов. Для производства окисленных углей в промышленных масштабах возможно использование в качестве сырья как ископаемых (бурых или каменных) углей, так и растительных углей.
При окислении углей изменяется выход летучих веществ и элементный состав, происходит снижение теплоты сгорания и ухудшение спекаемости, снижается выход продуктов коксования (смолы, сырого бензола и газа) и снижается теплота сгорания коксового газа [1]. Для бурых углей характерно резкое возрастание содержания гуминовых кислот, в каменных углях появляются вторичные гуминовые кислоты [2].
Изучение наиболее простого способа окисления угля – воздухом или кислородом при обыкновенной температуре – первоначально было связано с проблемой потери качества угля при хранении. Процессы автоокисления исследованы в аспекте изучения явлений выветривания и самовозгорания, а также изменения свойств углей, как конечной продукции. Эти исследования, в основном, проводились для каменных углей. Если процесс окисления идет быстро, то выделяющееся тепло не успевает уходить и возникает самовозгорание угля, которое выводит из строя шахты и уничтожает большие угольные массивы. Когда окисление идет медленно, то процесс не доходит до самовозгорания, но качество угля меняется, причем именно в сторону ухудшения.
Окисление углей объясняется двумя группами факторов: химическими и физическими. Первые следует считать основными: под влиянием кислорода происходит изменение или даже частичное разложение органической массы угля, ведущее к указанным переменам в химических и физических свойствах по сравнению с первоначальными. Физические факторы, способствующие окислению, следует считать второстепенными. Это в основном явления, ведущие к измельчению угля [4].
Направленная окислительная деструкция как каменных, так и бурых углей различными окислителями первоначально осуществлялась с целью познания их химического строения, так как эта реакция в дополнении с гидролизом позволяет получить более простые их фрагменты и идентифицировать их. В дальнейшем окисление стало рассматриваться уже как основа технологического процесса получения различных химических продуктов, необходимых для народного хозяйства. Выход и состав продуктов зависят от генетической природы твердых горючих ископаемых, окислителя и условий процесса [3].
По глубине влияния на угольное вещество процесс окисления можно разделить на три стадии [6]. Первая стадия окисления – поверхностное окисление, когда наблюдается присоединение кислорода с образованием на поверхности угля групп, обладающих кислотными свойствами. Скорость, с которой протекает этот процесс, определяется степенью углефикации, температурой, парциальным давлением кислорода и суммарной поверхностью частиц. На этой стадии не образуется продуктов, растворимых в щелочи. На второй стадии окисления значительная часть органического вещества угля превращается в продукты, растворимые в щелочи, образуются так называемые «регенерированные» гуминовые кислоты. При третьей стадии продукты окисления становятся растворимыми не только в щелочи, но и в воде с получением кислот. Окислению наиболее подвержены бурые и, в меньшей степени, каменные угли [7].
К изучению влияния процесса предварительного окисления органической массы бурых углей на эффективность их переработки в гуминовые вещества подтолкнул тот факт, что бурые угли являются уникальным природным образованием, в котором в процессе трансформации органической массы сформировалось специфическое вещество – гуминовые кислоты, – составляющее значительную (20–30 %), а в ряде случаев преобладающую (до 80–90 %) часть. А по своей природе гуминовые кислоты являются высокоокисленными, мало- или практически негорючими органо-минеральными веществами. Это и объясняет то, что бурые угли является преимущественно не энергоносителями, а источниками гуминовых кислот.
Трудность изучения механизма окисления органической массы углей заключается в сложности и неоднозначности строения состава и структуры вещества углей (органического и неорганического). Это влечет за собой сложность и неоднозначность химических реакций, протекающих при окислении твердых горючих ископаемых. В этом случае способ изучения данного процесса приобретает экспериментально-статистический характер с выделением общих закономерностей. Однако изучение окисления даже на таком уровне имеет большое теоретическое значение в области изучения химической структуры угля.
Приведенные выше сведения позволяют сделать вывод о том, что искусственное окисление углей различными окислителями позволяет повысить выход гуминовых кислот, т.е. продуктов, растворимых в щелочной среде (например, в едком натре или калии). При этом условия процесса могут быть достаточно мягкие (атмосферное давление, невысокие температуры).
В качестве сырья был взят бурый уголь Харанорского месторождения. Харанорское буроугольное месторождение расположено в Забайкальском крае, в Борзинском районе. Угли по генетической классификации являются бурыми, гумусовыми. По ГОСТу относятся к технологической группе 1–2 Б. Выход гуминовых кислот по месторождению достаточно низкий и колеблется в пределах от 6 % до 17 % на сухое топливо при среднем значении 11,7 %.
Проба угля, взятая для проведения экспериментальных работ по окислению имела следующие показатели технического анализа: Wa = 6,6 %; Ad = 7,3 %; Vdaf = 45,4 %. Выход свободных гуминовых кислот изучаемой пробы низкий и составлял (НА)f = 6,7 %, низшая теплота сгорания 21,2 Дж/кг.
В процессе работы, целью которой являлось определение степени влияния процесса предварительного окисления органической массы бурых углей на эффективность их переработки в гуминовые вещества, изучалось влияние различных окислителей на изменение выхода гуминовых кислот из бурых углей, а также зольности и теплоты сгорания.
В качестве реагентов при изучении влияния окисления были выбраны окислители разных классов и силы:
– неорганические окислители: соляная, фосфорная, серная и азотная кислоты, пероксид водорода, перманганат калия, озон;
– органические окислители: уксусная и лимонная кислоты.
Основной ход экспериментальных работ по окислению сырья состоял в следующем. Пробу сырья, измельченного до размера менее 0,2 мм, заливали окисляющим реагентом, в среде которого уголь оставляли на определенное условиями эксперимента время. По истечении запланированного времени пробу перемещали на фильтр, промывали водой и сушили до воздушно-сухого состояния. После чего проводили технический анализ с определением влажности, зольности, выхода летучих веществ и выхода гуминовых кислот.
Проведенные эксперименты показали, что действие сильной (соляной) и слабой (фосфорной) неорганических кислот на степень окисления органической массы углей практически сопоставимо с действием слабых органических (уксусной и лимонной) кислот тех же концентраций (рис. 1). При этом в общем случае при повышении концентрации окислителя выход гуминовых веществ увеличивается. Наибольшее повышение выхода гуминовых кислот отмечено при окислении углей пероксидом водорода при концентрации 6–10 %.
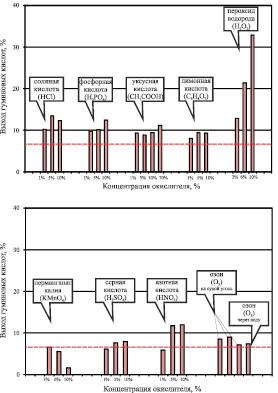
Рис. 1. Выход гуминовых кислот из бурого угля Харанорского месторождения при окислении различными реагентами (- - - – уровень гуминовых кислот в неокисленном угле)
Окисление перманганатом калия (рис. 1), являющимся общеизвестным сильным окислителем, не привело к увеличению выхода гуминовых кислот, а наоборот, отмечено снижение этого показателя. С увеличением концентрации перманганата калия выход гуминовых кислот заметно снижается. Следовательно, воздействие таким окислителем на органическую массу угля Харанорского месторождения привело к разрушению гуминовых кислот в составе органической массы, чем и объясняется снижение их содержания.
Серная и азотная кислоты (рис. 1) также показали небольшое воздействие по увеличению исследуемого показателя. Для бурого угля Харанорского месторождения эти кислоты при концентрации 1 % ведут к снижению, а при 5 и 10 %-ой концентрации ведут к повышению выхода гуминовых кислот, при этом азотная кислота более эффективна.
В качестве окислителя угля харанорского месторождения в данном цикле экспериментов использовался озон. Озон вырабатывался аппаратом газовой озонотерапии «Озотрон» с концентрацией озона на выходе из аппарата 1–7 г/м3. Окисление озоном было проведено в двух вариантах: подача газа через слой сухого угля и подача газа в смесь угля с водой. Оба метода не показали высокого увеличения выхода гуминовых кислот (рис. 1).
В процессе взаимодействия с углем окисляющие реагенты вступают в реакции не только с органической (угольное вещество), но и с неорганической составляющей (золой). В зависимости от типа реагента, его силы, а также состава золы действие реагентов на зольную составляющую различно. Для бурого угля Харанорского месторождения снижение зольности (рис. 2) происходит в той или иной степени, при действии всех рассматриваемых реагентов, кроме перманганата калия и озона.
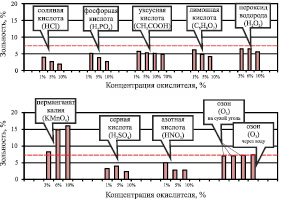
Рис. 2. Зольность бурого угля Харанорского месторождения при окислении различными реагентами (- - - – зольность неокисленного угля)
Действие окислителей на органическую массу, как отмечалось выше, также можно оценить снижением теплоты сгорания. На рис. 3 приведены результаты определения теплоты сгорания окисленных в ходе эксперимента проб, которые отображены в виде процентного снижения этого показателя относительно его начального значения для удобства отображения результатов. Наибольшее снижение теплоты сгорания отмечено при окислении соляной кислотой (10 %) и пероксидом водорода (10 %), что совпадает с результатами изучения эффективности окисления по выходу гуминовых кислот, где именно эти два окислителя показали наилучший результат.
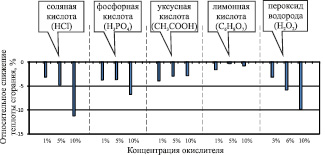
Рис. 3. Относительное снижение теплоты сгорания бурого угля Харанорского месторождения при окислении различными реагентами
Для изучения влияния времени окисления на изменение качественных показателей сырья пробы окислялись в течение 1 и 24 часов, при этом лишь в некоторых случаях отмечалось незначительное увеличение выхода гуминовых кислот (рис. 4, а) и незначительное снижение зольности угля (рис. 4, б) с увеличением времени окисления.
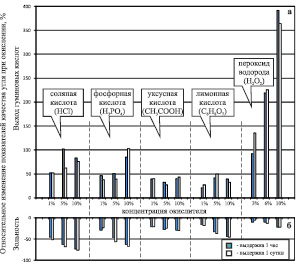
Рис. 4. Сравнение относительного изменения выхода гуминовых кислот и зольности при изменении времени окисления бурого угля Харанорского месторождения
В итоге проведенных экспериментальных исследований под действием практически всех выбранных реагентов-окислителей отмечено повышение выхода гуминовых кислот, снижение зольности, снижение теплотворной способности бурых углей Харанорского месторождения. Таким образом, все исследуемые реагенты-окислители в той или иной степени имеют окисляющее действие на органическую массу бурого угля и приводят к повышению выхода гуминовых веществ. Наибольший эффект отмечен при использовании для окисления пероксида водорода при концентрации 6–10 %, а также соляной кислоты при концентрации 10 %. При сопоставимых результатах действия этих двух реагентов предпочтительнее является применение пероксида водорода по условиям безопасности применения. Кроме того, после проведения окисления уголь необходимо промыть, так как для дальнейшего извлечения гуминовых веществ следует щелочная обработка угля. В случае применения неорганических кислот (соляной, фосфорной и др.) промывка угля до нейтральной реакции занимает значительное время и требует большого количества воды. Пероксид водорода промывается значительно легче, кроме того, этот реагент разлагается при нагреве до температуры выше 70–75 °С, что также является неоспоримым преимуществом.
Результаты проведенных экспериментальных исследований по изучению влияния предварительного окисления угля могут быть положены в основу нового способа переработки бурых углей в гуминовые вещества.
Библиографическая ссылка
Москаленко Т.В., Михеев В.А., Ворсина Е.В. ПОВЫШЕНИЕ ИЗВЛЕЧЕНИЯ ГУМИНОВЫХ ВЕЩЕСТВ ИЗ БУРОГО УГЛЯ ХАРАНОРСКОГО МЕСТОРОЖДЕНИЯ НАПРАВЛЕННЫМ ОКИСЛЕНИЕМ // Современные наукоемкие технологии. 2016. № 2-3. С. 435-440;URL: https://top-technologies.ru/en/article/view?id=35648 (дата обращения: 14.05.2026).



