Введение
Твердые растворы на основе ферритов и хромитов никеля (II) находят широкое применение в технике в качестве магнитных и полупроводниковых материалов. Изучению вопроса формирования структуры шпинели посвящено много исследований. Однако до настоящего времени до конца не выявлены факторы, влияющие на скорость и полноту формирования структуры шпинели. Целью настоящего исследования являлось изучение механизма образования твердых растворов в системе NiFe2-xCrxO4, (х = 1,4; 1,6; 2,0) в ходе топохимической реакции.
Материалы и методы исследования
Для приготовления образцов твердых растворов NiFe2-xCrxO4 были составлены сырьевые смеси из оксидов железа (III), хрома (III) и никеля (II) марки хч, отвечающие стехиометрическому соотношению компонентов NiO, Fe2O3, Cr2O3 в твердых растворах шпинелей. Исходные оксиды имели размер зерна не более 0,1 мм (проходили через сито 10000 отв/см2). Подробно методика синтеза материалов изложена в [3, 5-7]. Полноту синтеза контролировали с помощью рентгенофазового анализа (РФА) на рентгеновском дифрактометре ДРОН-3. Для идентификации фаз использовали картотеку ASTM, параметры элементарных ячеек определяли по линии (440) (кубическая фаза), (440) и (404) (тетрагональная фаза). Рентгенограммы образцов приведены на рис. 1.
Результаты исследования
и их обсуждение
В ходе проводимого исследования установлено, что синтез образцов состава NiFe0,6Cr1,4O4 завершен полностью, для NiFe0,4Cr1,6O4 процесс прошел на 96%, хромита никеля (II) NiCr2O4 в образце – 90%.
На процесс формирования структуры шпинели оказывают влияние многие факторы, их можно условно разбить на две группы. К первой относятся факторы, определяющиеся составом и структурой образующегося кристалла (энергия кристаллической решетки, плотность, температура плавления и т.д.). Ко второй группе – факторы, связанные с наличием примесей и дефектов кристаллической решетки (диффузия, механическая прочность, пластическая деформация и т.д.).
Как известно [2], энергия кристаллической решетки представляет собой ту работу, которую нужно совершить, чтобы разорвать связи, действующие между структурными единицами. Эта величина характеризует прочность связей в кристалле и его устойчивость.
Расчет энергии кристаллической решетки (W) был проведен по уравнению Капустинского по методике, изложенной в [1]:

Рис. 1. Рентгенограмма образцов в системе NiFe2-xCrxO4.
Индексированы линии, принадлежащие шпинели
Рассчитанные значения энергии кристаллических решеток U исходных оксидов и образующихся шпинелей приведены в табл. 1.
Таблица 1
Величина энергии
кристаллической решетки
|
Формульная единица вещества |
U, кДж/моль |
|
NiO |
3831 |
|
Fe2O3 |
14761 |
|
Cr2O3 |
14937 |
|
NiFe0,6Cr1,4O4 |
18590 |
|
NiFe0,4Cr1,6O4 |
18602 |
|
NiCr2O4 |
18632 |
Примечание. Для шпинелей rк рассчитывали по формуле:
rк = 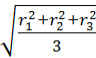 ,
,
где r1, r2, r3 – радиусы катионов, входящих в формульную единицу вещества, Ǻ.
Согласно полученным данным, наименьшей энергией решетки обладает исходный оксид никеля (II). В этой связи можно предположить, что диффузионные процессы будут осуществляться за счет катиона Ni2+. Однако в [7] для хромита никеля (II) было отмечено, что процесс формирования структуры протекает за счет диффузии Cr3+.
Для объяснения экспериментально наблюдаемых зависимостей следует допустить влияние структурного фактора на скорость диффузионных процессов. Оксид никеля (II) кристаллизуется в кубической решетке типа NaCl (пространственная группа Fm3m) [4,8]. Она характеризуется гранецентрированной ячейкой Бравэ, каждый ион Ni2+ окружен шестью ионами O2-. В такой структуре имеются взаимопроникающие две плотнейшие упаковки: одна – из атомов никеля, другая – из атомов кислорода. Катионы никеля занимают все октаэдрические пустоты. Для стехиометрического NiO число ионов никеля равно числу ионов кислорода, следовательно, в структуре заполнены все октаэдрические пустоты, а тетраэдрические остаются свободными. Вероятно, диффузия катионов никеля из узлов более совершенной кубической решетки затруднена, и формирование шпинельной структуры протекает за счет катионов трехвалентных металлов. Оксиды Fe2O3 и Cr2O3 имеют ромбоэдрическую решетку типа корунда (α-Al2O3, пространственная группа R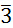 c). Ее можно описать как искаженную ромбоэдрически структуру NaCl, в которой атом натрия или хлора заменен на группу Al2O3. В такой структуре ионы кислорода образуют ориентировочно гексагональную плотнейшую упаковку, а катионы металла заполняют 2/3 октаэдрических пустот, лежащих в направлении <10
c). Ее можно описать как искаженную ромбоэдрически структуру NaCl, в которой атом натрия или хлора заменен на группу Al2O3. В такой структуре ионы кислорода образуют ориентировочно гексагональную плотнейшую упаковку, а катионы металла заполняют 2/3 октаэдрических пустот, лежащих в направлении <10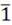 0> [8]. По-видимому, диффузия катионов металла по оставшимся свободным узлам кристаллической решетки протекает легче. Кроме того, можно предположить, что в случае составов, обогащенных Fe3+, формирование структуры шпинели будет происходить преимущественно за счет диффузии трехвалентного катиона железа (III), поскольку энергия кристаллической решетки Fe2O3 ниже, чем у Cr2O3 (см. табл. 1). В связи с этим, следовало ожидать увеличения продолжительности синтеза шпинелей NiFe2-хCrхO4 с увеличением х (то есть, при уменьшении содержания Fe3+ в составе шпинели). Такая зависимость в скорости формирования структуры шпинели экспериментально наблюдалась для изученных составов рассматриваемой системы.
0> [8]. По-видимому, диффузия катионов металла по оставшимся свободным узлам кристаллической решетки протекает легче. Кроме того, можно предположить, что в случае составов, обогащенных Fe3+, формирование структуры шпинели будет происходить преимущественно за счет диффузии трехвалентного катиона железа (III), поскольку энергия кристаллической решетки Fe2O3 ниже, чем у Cr2O3 (см. табл. 1). В связи с этим, следовало ожидать увеличения продолжительности синтеза шпинелей NiFe2-хCrхO4 с увеличением х (то есть, при уменьшении содержания Fe3+ в составе шпинели). Такая зависимость в скорости формирования структуры шпинели экспериментально наблюдалась для изученных составов рассматриваемой системы.
Выводы
В ходе изучения процессов формирования структуры твердых растворов NiFe2-xCrxO4 выявлено, что продолжительность синтеза зависит от содержания катионов Fe3+ в составе твердого раствора. С уменьшением содержания катионов Fe3+ в составе твердого раствора продолжительность синтеза увеличивается. Высказано предположение, что на процесс образования шпинели в результате топохимической реакции оказывают кристаллохимические особенности исходных оксидов.
Библиографическая ссылка
Шабельская Н.П., Захарченко И.Н., Ульянов А.К. О МЕХАНИЗМЕ ОБРАЗОВАНИЯ ФЕРРИТОВ-ХРОМИТОВ НИКЕЛЯ (II) В ХОДЕ ТОПОХИМИЧЕСКОГО ПРОЦЕССА // Современные наукоемкие технологии. 2014. № 3. С. 150-152;URL: https://top-technologies.ru/ru/article/view?id=34131 (дата обращения: 27.04.2026).



